Hòa tan hết hỗn hợp gồm 7,2 gam Mg và 22,4 gam Fe trong 500 ml dung dịch Fe(NO3)3 x mol/l và Cu(NO3)2 y mol/l thu được dung dịch X và 31,2 gam chất rắn Y gồm 2 kim loại. Để tác dụng tối đa với dung dịch X cần dung dung dịch chứa 2,0 mol NaOH (không có không khí). Giá trị x, y là
A. 0,4M và 0,8M
B. 0,6M và 0,45M
C. 0,8M và 0,8M
D. 0,8M và 0,6M



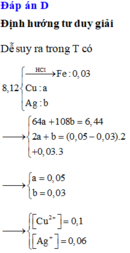

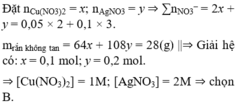

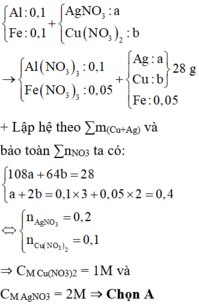
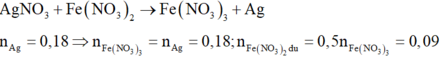

Đáp án C
nMg=0,3 mol; nFe=0,4 mol; nFe(NO3)3=0,5x mol; nCu(NO3)2=0,5y
Do Y gồm 2 kim loại (Cu, Fe) nên Mg hết, Fe dư, Fe(NO3)3 hết; Cu(NO3)2 hết
+ X gồm: 0,3 mol Mg(NO3)2 và a mol Fe(NO3)2
nNaOH=2nMg(NO3)2+2nFe(NO3)2=>2=2.0,3+2.a=>a=0,7mol
+ Y gồm (Cu: 0,5y mol; Fe dư: 0,5x+0,4-0,7=0,5x-0,3 mol) => 64.0,5y+56.(0,5x-0,3)=31,2 (1)
+ BTNT N: 3nFe(NO3)3+2nCu(NO3)2=2nMg(NO3)2+2nFe(NO3)2 => 3.0,5x+2.0,5y=2.0,3+2.0,7 (2)
Giải (1) và (2) => x=0,8M; y=0,8M
Giả sử chúng ta có hỗn hợp gồm 7,2 gam Mg và 22,4 gam Fe. Khi hòa tan hỗn hợp này trong dung dịch Fe(NO3)3 và Cu(NO3)2, ta thu được dung dịch X và 31,2 gam chất rắn Y gồm 2 kim loại.
Để tác dụng tối đa với dung dịch X, chúng ta cần dung dịch chứa 2,0 mol NaOH (không có không khí).
Chúng ta cần xác định giá trị của x và y.
Bước 1: Xác định số mol của Mg và Fe trong hỗn hợp ban đầu:
Số mol Mg: (n_{\text{Mg}} = \frac{{\text{khối lượng Mg}}}{{\text{khối lượng molecul Mg}}} = \frac{{7,2}}{{24,31}})Số mol Fe: (n_{\text{Fe}} = \frac{{\text{khối lượng Fe}}}{{\text{khối lượng molecu Fe}}} = \frac{{22,4}}{{55,85}})Bước 2: Xác định số mol của Fe(NO3)3 và Cu(NO3)2:
Số mol Fe(NO3)3: (n_{\text{Fe(NO3)3}} = x \times 0,5)Số mol Cu(NO3)2: (n_{\text{Cu(NO3)2}} = y \times 0,5)Bước 3: Xác định số mol của Mg(NO3)2 và Fe(NO3)2 sau phản ứng:
Số mol Mg(NO3)2: (n_{\text{Mg(NO3)2}} = n_{\text{Mg}} - n_{\text{Fe(NO3)3}})Số mol Fe(NO3)2: (n_{\text{Fe(NO3)2}} = n_{\text{Fe}} - n_{\text{Cu(NO3)2}})Bước 4: Xác định số mol của NaOH cần để tác dụng với Mg(NO3)2:
Số mol NaOH: (n_{\text{NaOH}} = 2,0)Bước 5: Xác định số mol của Mg(OH)2 sau phản ứng:
Số mol Mg(OH)2: (n_{\text{Mg(OH)2}} = n_{\text{Mg(NO3)2}})Bước 6: Tính giá trị của x:
(n_{\text{Mg(OH)2}} = n_{\text{Mg(NO3)2}})(n_{\text{Mg(OH)2}} = n_{\text{Mg}} - n_{\text{Fe(NO3)3}})(2,0 = \frac{{7,2}}{{24,31}} - x \times 0,5)Giải phương trình trên để tìm x.Bước 7: Tính giá trị của y:
(n_{\text{Cu(NO3)2}} = n_{\text{Fe}} - n_{\text{Fe(NO3)2}})(y \times 0,5 = \frac{{22,4}}{{55,85}} - x \times 0,5)Giải phương trình trên để tìm y.Sau khi tính toán, ta có:
(x \approx 0,8M)(y \approx 0,6M)Vậy giá trị của x và y là 0,8M và 0,6M