: Phân tích một mẫu hợp chất tạo bởi 2 nguyên tố là Fe và O. Kết quả cho thấy cứ 7 phần khối lượng Fe có tương ứng với 3 phần khối lượng oxi.
a. Viết công thức hóa trị của Fe trong hợp chất
b. Xác định hóa trị của Fe trong hợp chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTHH : Fe2O3
hóa trị :
a . x = y.b
=> a .2 = 2.3
=> a = lll

Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
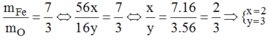
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)

Gọi CTHH của HC là FexOy
Ta có:
nFe trong HC=7:56=0,125
nO trong HC=3:16=0,1875
=>\(\dfrac{x}{y}=\dfrac{0,125}{0,1875}=\dfrac{2}{3}\)
Vậy CTHH của HC là Fe2O3
Gọi a là hóa trị của Fe trong HC
Theo quy tắc hóa trị ta có:
a.2=II.3
=>a=3
Vậy Fe hóa trị 3 trong HC Fe2O3

Hợp chất Fe2O3. Gọi hóa trị của Fe là x
Theo quy tắc hóa trị ta có: x. 2 = 3.II ⇒ x = III

a) Đặt công thức chung : FexOy
\(\dfrac{m_{Fe}^{ }}{m_O}=\dfrac{56x}{16y}=\dfrac{7}{3}\)
168x=112y
\(\dfrac{x}{y}=\dfrac{112}{168}=\dfrac{2}{3}\)
=> x=2 ; y=3
Vậy công thức hóa học : Fe2O3
PKt : 56.2 + 16.3 = 160 (đvC)
b) Gọi hóa trị của Fe là x
Ta có : x.2 = II . 3
=> x = \(\dfrac{II.3}{2}=III\)
Vậy hóa trị của FE là III.

a ) Đặt công thức hóa học của hợp chất có dạng chung là FexOy.Ta có :
\(\%m_{Fe}=\frac{56x}{56x+16y}\times100\%=72,414\%\Rightarrow\frac{x}{y}=\frac{3}{4}\Rightarrow x=3\) và \(y=4\)
\(\Rightarrow\) CTHH của hợp chất là : \(Fe_3O_4.\)
\(\Rightarrow\) PTK của \(Fe_3O_4\)là \(56\times3+4\times16=232\) đvC
b ) \(Fe_3O_4=FE^{II}O^{II}.Fe_2^{III}O_3^{II}\)
\(\Rightarrow\) Trong phân tử Fe3O4 thì Fe có hóa trị II và III .
Vậy x=2, y=3
Công thức hóa học của hợp chất là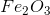
Phân tử khối bằng
b) Hóa trị của Fe trong hợp chất là : III