Hòa tan hỗn hợp gồm Fe và FeS vào dung dịch HCl dư, thu được 8,96 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 dư thì thu được 23,9 gam kết tủa đen. Khối lượng Fe trong hỗn hợp đầu là:
A. 11,2
B. 16,8
C. 5,6
D. 8,4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{PbS}=\dfrac{47,8}{239}=0,2\left(mol\right)\)
Bảo toàn S: \(n_{FeS}=n_{H_2S}=0,2\left(mol\right)\)
\(n_{H_2}=\dfrac{6,72}{22,4}-0,2=0,1\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<----------------------0,1
=> mFe = 0,1.56 = 5,6 (g)
mFeS = 0,2.88 = 17,6 (g)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{5,6+17,6}.100\%=24,138\%\\\%m_{FeS}=\dfrac{17,6}{5,6+17,6}.100\%=75,862\%\end{matrix}\right.\)

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> mFe = 0,2.56 = 11,2 (g)
\(n_{CuS}=\dfrac{9,6}{96}=0,1\left(mol\right)\)
PTHH: Cu(NO3)2 + H2S --> CuS + 2HNO3
0,1<---0,1
FeS + 2HCl --> FeCl2 + H2S
0,1<---------------------0,1
=> mFeS = 0,1.88 = 8,8 (g)
=> m = 11,2 + 8,8 = 20 (g)

nhh=0,11 mol
n PbS=0,1 mol
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.

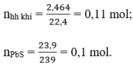
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.

`Fe + 2HCl -> FeCl_2 + H_2 ↑`
`0,2` `0,2` `(mol)`
`FeS + 2HCl -> FeCl_2 + H_2 S↑`
`0,1` `0,1` `(mol)`
`H_2 S + Pb(NO_3)_2 -> PbS↓ + 2HNO_3`
`0,1` `0,1` `(mol)`
`n_[PbS] = [ 23,9 ] / 239 = 0,1 (mol)`
`n_Y = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
`a)` Hỗn hợp `Y` gồm khí `H_2` và `H_2 S`
`=> n_[H_2 S] = 0,1 (mol)`
`=> n_[H_2] = 0,3 - 0,1 = 0,2 (mol)`
`b)m_[hh] = 0,2 . 56 + 0,1 . 88 = 20 (g)`

a, PT: \(FeS+2HCl\rightarrow FeCl_2+H_2S\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(H_2S+Pb\left(NO_3\right)_2\rightarrow2HNO_3+PbS_{\downarrow}\)
b, Hỗn hợp khí thu được gồm: H2, H2S.
Ta có: \(n_{PbS}=\dfrac{23,9}{239}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2S}=n_{PbS}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2}=\dfrac{2,464}{22,4}-0,1=0,01\left(mol\right)\)
⇒ Tỉ lệ số mol H2: H2S = 0,01:0,1 = 1:10
c, Theo PT: \(\left\{{}\begin{matrix}n_{FeS}=n_{H_2S}=0,1\left(mol\right)\\n_{Fe}=n_{H_2}=0,01\left(mol\right)\end{matrix}\right.\)
⇒ mhh = mFeS + mFe = 0,1.88 + 0,01.56 = 9,36 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{FeS}=\dfrac{0,1.88}{9,36}.100\%\approx94,02\%\\\%m_{Fe}\approx5,98\%\end{matrix}\right.\)
Đáp án B