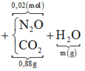
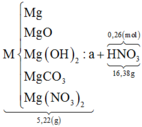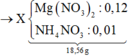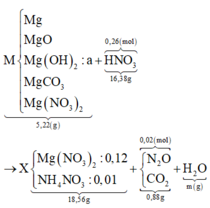Câu 12. Trung hòa vừa đủ 500ml dung dịch gồm NaOH 0,5M và Ba(OH)2 1M với dung dịch H2SO4 15%. Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng. Hãy :
a) Tính khối lượng dung dịch H2SO4 đã dùng .
b) Tính khối lượng chất kết tủa thu được.
c) Tính CM của Na2SO4 biết D H2SO4 = 1,14 g/cm3