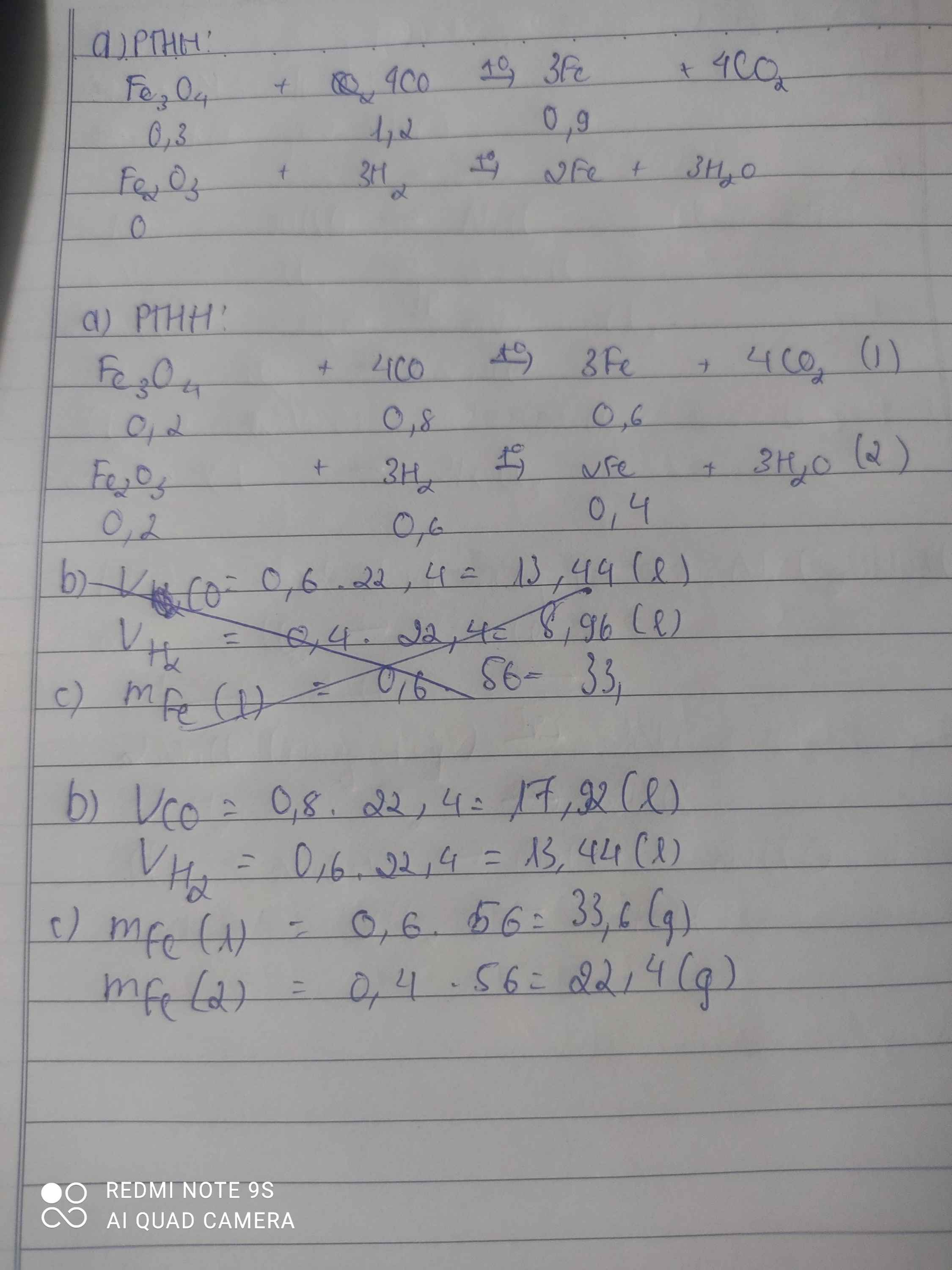Trong phòng thí nghiệm, người ta đã dùng cacbon oxit CO để khử 0,2 mol F e 3 O 4 và dùng khí hidro để khử 0,2 mol F e 2 O 3 ở nhiệt độ cao.
a. Viết phương trình hoá học của các phản ứng đã xảy ra
b. Tính số lít khí CO và H 2 ở đktc cần dùng cho mỗi phản ứng.
c. Tính số gam sắt thu được ở mỗi phản ứng hoá học.