Cho 22,4 gam sắt tác dụng với dung dịch loãng có chứa 24,5 gam axit sunfuric.
a) Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b) Tính thể tích khí hiđro thu được ở đktc.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)

a. PTHH :Fe + H2SO4 -> FeSO4 +H2
nFe = 22,4 : 56 = 0,4 (mol)
nH2SO4 = 24,5 : 98 = 0,25 (mol)
Ta có nFe > nH2SO4 (0,4>0,25) nên Fe dư
nFe dư = 0,4-0,25 = 0,15 (mol)
Vậy mFe dư = 0,15 . 56 = 8,4 (gam)
b, Theo PTHH ta có nH2 = nH2SO4 =0,25 (mol)
=> VH2 thu được (đktc) =0,25 . 22,4 =5,6(lit)
Ta có: \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\ n_{H_2SO_4\left(loãng\right)}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PTHH: Fe + H2SO4 (loãng) -> FeSO4 + H2\(\uparrow\)
Theo PTHH và đề bài, ta có:
\(\dfrac{n_{Fe\left(đềbài\right)}}{n_{Fe\left(PTHH\right)}}=\dfrac{0,4}{1}>\dfrac{n_{H_2SO_4\left(loãng,đềbài\right)}}{n_{H_2SO_4\left(loãng,PTHH\right)}}=\dfrac{0,25}{1}\)
=> H2SO4 loãng hết, Fe dư nên tính theo \(n_{H_2SO_4\left(loãng\right)}\)
Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Fe\left(phảnứng\right)}=n_{H_2SO_4\left(loãng\right)}=0,25\left(mol\right)\\ =>n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
a) Khối lượng Fe dư:
\(m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b) Thể tích khí H2 thu được (ở đktc):
\(V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)

\( n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,25 0 0
0,1 0,15 0,05 0,15
0 0,1 0,05 0,15
Chất \(H_2SO_4\) dư và dư \(m=0,1\cdot98=9,8g\)
\(V_{H_2}=0,15\cdot22,4=3,36l\)
\(nAl=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(nH_2SO_4=\dfrac{24,5}{98}=0,25\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,1---->0,15------>0,05--------------->0,15
Xét tỉ lệ : \(\dfrac{0,1}{2}< \dfrac{0,25}{3}\)
=> H2SO4 dư vs pứ
\(nH_2SO_{4\left(dư\right)}=0,25-0,15=0,1\left(mol\right)\)
\(mH_2SO_4=\)\(0,1.98=9,8\left(g\right)\)
\(VH_2=0,15.22,4=3,36\left(lít\right)\)

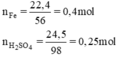
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 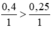 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.

a, \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b, \(n_{H_2}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)

a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Fe còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,25\left(mol\right)\\n_{Fe\left(dư\right)}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,25\cdot22,4=5,6\left(l\right)\\m_{Fe\left(dư\right)}=0,15\cdot56=8,4\left(g\right)\end{matrix}\right.\)
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
Pt : Fe + H2SO4 → FeSO4 + H2\(|\)
1 1 1 1
0,4 0,25 0,25
a) Lập tỉ số so sánh : \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\)
⇒ Fe dư , H2SO4 phản ứng hết
⇒ Tính toán dựa vào số mol của H2SO4
Số mol của khí hidro
nH2 = \(\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
Thể tích của khí hidro
VH2 = nH2 . 22,4
= 0,25 . 22,4
= 5,6 (l)
b) Số mol dư của sắt
ndư = nban đầu - nmol
= 0,4 -(0,25 . 1)
= 0,15 (mol)
Khối lượng dư của sắt
mdư = ndư . MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt

nFe = 22.4/56 = 0.4 (mol)
nH2SO4 = 24.5/98 = 0.25 (mol)
Fe + H2SO4 => FeSO4 + H2
0.25.....0.25.....................0.25
mFe(dư) = ( 0.4 - 0.25 ) * 56 = 8.4 (g)
VH2 = 0.25 * 22.4 = 5.6 (l)
nFe=\(\dfrac{22,4}{56}\)= 0,4 ( mol)
nH2SO4=\(\dfrac{24,5}{98}\)=0,25 ( mol )
Fe + H2SO4 → FeSO4 + H2
Trước phản ứng: 0,4 0,25 ( mol )
Phản ứng: 0,25 0,25 0,25 ( mol )
Sau phản ứng: 0,15 0,25 0,25 ( mol )
a) m= n.M= 0,15.56=8,4 (g)
vậy Fe còn dư và dư 8,4 gam
b) VH2= n.22,4= 0,25.22,4=5,6 (l)

a, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=n_{Fe}=0,2\left(mol\right)\Rightarrow n_{H_2SO_4\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,1.98=9,8\left(g\right)\)
b, \(n_{H_2}=n_{Fe}=0,2\left(mol\right)\Rightarrow n_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,2}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,2\left(mol\right)\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)