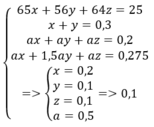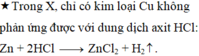Hỗn hợp X gồm Mg, Al, Fe, Cu trong đó số mol Fe gấp đôi số mol Cu. Lấy 21,4 g X td với dd HCl dư , sau pư hoàn toàn thu được 15,68 l khí (đktc) Nếu lấy 10,7 g X cho phản ứng hết với khí Cl2 -> 39,1 g muối. Tính % khối lượng Fe và Cu trong hỗn hợp ban đầu.( Giải chi tiết nha)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giả sử 21,4 gam X chứa \(\left\{{}\begin{matrix}Cu:a\left(mol\right)\\Fe:2a\left(mol\right)\\R:b\left(mol\right)\end{matrix}\right.\)
=> 176a + b.MR = 21,4 (1)
\(n_{H_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
2a--------------------->2a
2R + 2nHCl --> 2RCln + nH2
b---------------------->0,5bn
=> 2a + 0,5bn = 0,7 (2)
- 10,7g X chứa \(\left\{{}\begin{matrix}Cu:0,5a\left(mol\right)\\Fe:a\left(mol\right)\\R:0,5b\left(mol\right)\end{matrix}\right.\)
\(n_{Cl_2}=\dfrac{39,1-10,7}{71}=0,4\left(mol\right)\)
PTHH: Cu + Cl2 --to--> CuCl2
0,5a->0,5a
2Fe + 3Cl2 --to--> 2FeCl3
a-->1,5a
2R + nCl2 --to--> 2RCln
0,5b->0,25bn
=> 2a + 0,25bn = 0,4 (3)
(2)(3) => a = 0,05 (mol); bn = 1,2
=> \(\left\{{}\begin{matrix}n_{Cu}=0,05\left(mol\right)\\n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,05.64}{21,4}.100\%=14,95\%\\\%m_{Fe}=\dfrac{0,1.56}{21,4}.100\%=26,17\%\end{matrix}\right.\)

Coi hỗn hợp X gồm R ( có hoá trị n - a mol) và Fe (b mol)
$\Rightarrow Ra + 56b = 6$
$2R + 2nHCl \to 2RCl_n + nH_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = 0,5an + b = \dfrac{1,85925}{22,4} = 0,083(mol)(1)$
$2R + nCl_2 \xrightarrow{t^o} 2RCl_n$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$m_{Cl_2} = m_{muối} - m_X = 12,39 - 6 = 6,39(gam)$
$n_{Cl_2} = 0,5an + 1,5b = 0,09(2)$
Từ (1)(2) suy ra : an = 0,138 ; b = 0,014
$\%m_{Fe} = a\% = \dfrac{0,014.56}{6}.100\% = 13,07\%$

Đáp án C
Đặt số mol mỗi kim loại trong 18,5 gam hỗn hợp lần lượt là a, b, c.
Ta có: mhh X =65a + 56b + 64c; n H 2 = a + b = 3 , 92 22 , 4 = 0 , 175 mol
Có số phân tử Cl2 phản ứng trung bình với hỗn hợp X:
n Cl 2 n X = 0 , 175 0 , 15 = 7 6 = ( a + 1 , 5 b + c ) ( a + b + c )
Từ đó ta có a - 2b + c = 0.
Tóm lại ta sẽ có a = b = c = 0,1 mol.
Vậy trong 18,5g hỗn họp X sẽ có 0,1 mol Fe
Chú ý:
Dung dịch axit như dung dịch HCl, HBr, HI hoặc dung dịch H2SO4 có khả năng phản ứng với các kim loại đứng trước H trong dãy điện hóa, tức là trong bài này phản ứng với Zn và Fe tạo ra ZnCl2 và FeCl2.
- Clo có khả năng phản ứng với hầu hết các kim loại (trừ Au, Pt) thậm chí còn có khả năng phản ứng với Ag ở điều kiên thích hợp và đưa kim loại lên số oxi hóa cao nhất vì vậy sản phẩm là ZnCl2,CuCl2,FeCl3

Đáp án : D
Gọi số mol Mg = Fe = x ; số mol Al = y ; số mol Cu = z trong X
=> 80x + 27y + 64z = 7,5g
2 n H 2 = 2nMg + 2nFe + 3nAl
=> 4x + 3y = 0,46 mol
Khi cho 1 lượng vừa đủ Mg(NO3)2 để phản ứng với Cu và Fe2+
tạo khí không màu hóa nâu trong không khí (NO)
=> NO3- chuyển hoàn toàn thành NO
=> bảo toàn e : 2nCu + n F e 2 + = 3nNO = 3 n N O 3
=> n N O 3 = (2z + x)/3 mol
=> n M g N O 3 2 = (x + 2z)/6 (mol)
=> Khi phản ứng với NaOH tạo kết tủa gồm :
x mol Fe(OH)3 ; [x + (x + 2z)/6 ] mol Mg(OH)2 và z mol Cu(OH)2
=> 9,92g = 524x/3 + 352z/3
=> x = 0,04 ; y = 0,1 ; z = 0,025 mol
=>%mFe(X) = 29,87%

\(n_{Cu} = a ; n_{Al} = b ; n_{Fe} = c(mol)\\ \Rightarrow 64a + 27b + 56c = 28,6(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5b + c = \dfrac{13,44}{22,4} = 0,6(2)\\ \text{Mặt khác} : n_{O_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3\\ \)
Ta có :
\(\dfrac{n_X}{n_{O_2}}=\dfrac{a+b+c}{0,5a +0,75b + 0,75c} = \dfrac{0,6}{0,4}(3)\\ (1)(2)(3)\Rightarrow a = \dfrac{317}{1460} ; b = \dfrac{121}{365}; c = \dfrac{15}{146}\\ \%m_{Cu} = \dfrac{\dfrac{317}{1460}.64}{28,6}.100\% = 48,59\%\\ \%m_{Al} = \dfrac{\dfrac{121}{365}.27}{28,6}.100\% = 31,3\%\\ \%m_{Fe} = 100\% - 41,59\% - 31,3\% = 27,11\%\)