1. Cho 32,4 gam kim loại nhôm phản ứng với 21,504 lít khí oxi (đktc).a. Tính khối lượng Al2O3 tạo thành.b. Tính khối lượng chất còn dư trong phản ứng.2. Cho 12,15 gam nhôm và một dung dịch có chứa 54 gam CuSO4.a. Chất nào dư sau phản ứng và dư bao nhiêu gam?b. Lọc bỏ chất rắn rồi đem cô cạn dung dịch thì thu được bao nhiêu gam muối khan?3. Nhiệt phân 29,4 gam kali clorata. Tính số milit khí oxi thu được.b. Nếu đốt 50,4...
Đọc tiếp
1. Cho 32,4 gam kim loại nhôm phản ứng với 21,504 lít khí oxi (đktc).
a. Tính khối lượng Al2O3 tạo thành.
b. Tính khối lượng chất còn dư trong phản ứng.
2. Cho 12,15 gam nhôm và một dung dịch có chứa 54 gam CuSO4.
a. Chất nào dư sau phản ứng và dư bao nhiêu gam?
b. Lọc bỏ chất rắn rồi đem cô cạn dung dịch thì thu được bao nhiêu gam muối khan?
3. Nhiệt phân 29,4 gam kali clorat
a. Tính số milit khí oxi thu được.
b. Nếu đốt 50,4 gam sắt trong lọ đựng lượng khí oxi trên, tính khối lượng sản phẩn thu được?
c. Lấy hết Fe3O4 trên tác dụng với lượng dư Hcl theo sơ đồ sau:
Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
Tính tổng khối lượng muối khan thu được sau khi cô cạn dụng dịch sau.
4. Cho 8,1 gam nhôm tác dụng với dung dịch có chứa 21,9 gam HCl.
a. Sau phản ứng chất nào còn dư, dư bao nhiêu gam?
b. Tính khối lượng AlCl3 thu được.
c. Khí sinh ra có thể khử được bao nhiêu gam CuO và thu được bao nhiêu gam Cu?



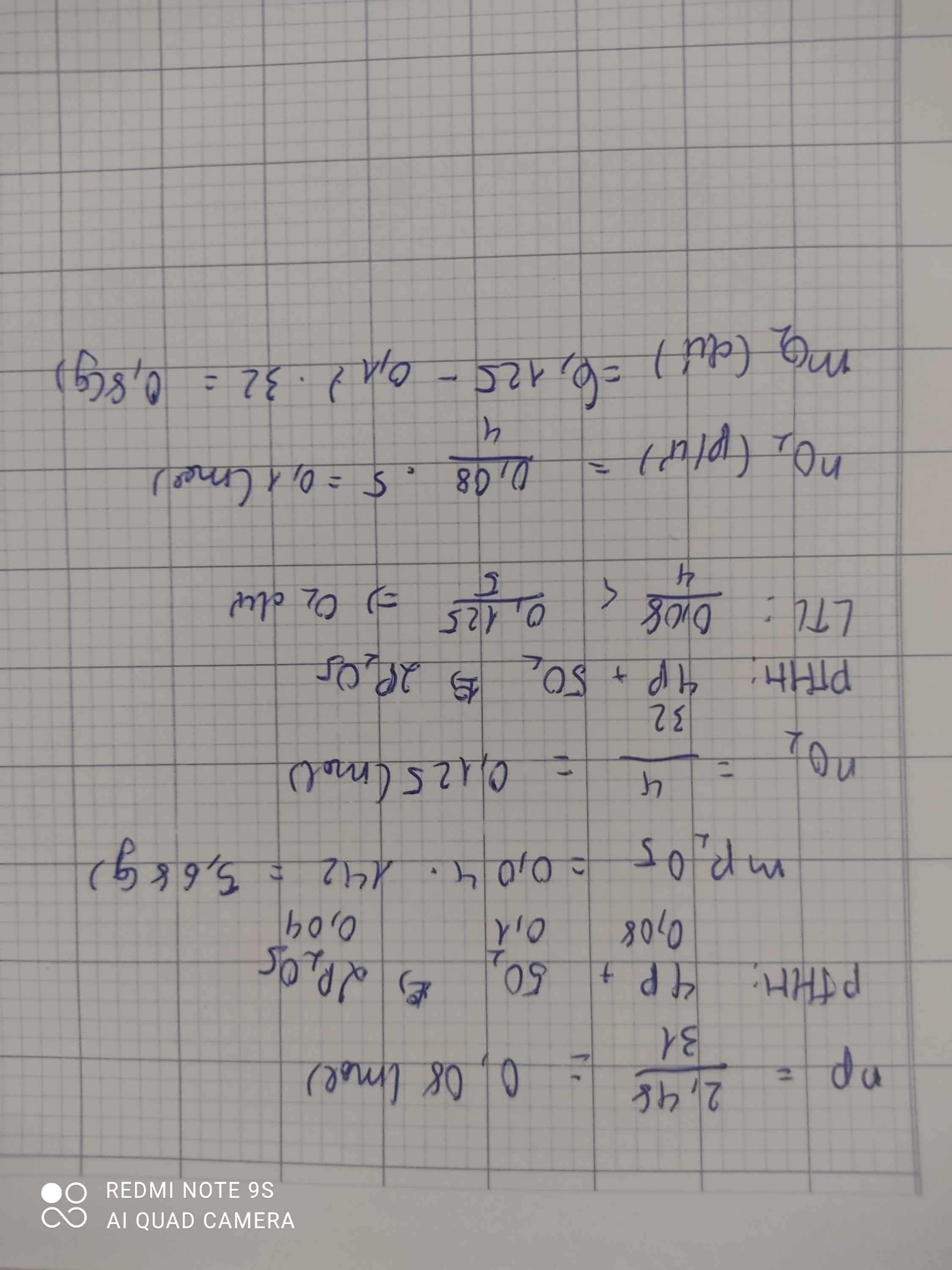


n Al = 0,2 mol
n O2 = 0,5 mol
4Al + 3O2 →2 Al2O3 t0 nữa nha
bđ o,2 0,5 mol
pứ 0,2 → 0,15→ 0,1 mol
sau pứ 0 0,35 0,1 mol
a. O2 dư =0,35.32=11,2 g
b. mAl2O3 = o,1.102=10,2 g