1 cốc thủy tinh đựng 300 gam dung dịch bão hòa KClO3 ở 20 độ ,C%=6,5 Làm bay hơi bớt nc r đưa dd cn lại về 20 độ , khối lượng cn lại trong cốc là 206,5 gam .Tính khối lượng KClO3 kết tinh và KClO3 trog dd cn lại
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng KClO3 tại 200C : \(\frac{600.6,5}{100}=39\left(g\right)\)
=> Khối lượng dung môi : \(600-39=561\left(g\right)\)
Ở 200C cứ 561g H2O hoà tan được 39g KClO3
=> Ở 200C 100g H2O hoà tan được 3,95 g KClO3
Khối lượng nước bay hơi là : \(600-413=187\left(g\right)\)
=> Khối lượng nước còn lại : \(561-187=374\left(g\right)\)
Ở 200C 100g H2O hoà tan được 3,95 g KClO3
=> Ở 200C 374 g H2O hoà tan được 26 g KClO3
=> Khối lượng chất rắn kết tinh : \(39-26=13\left(g\right)\)

Khối lượng KClO3 tại 200C : \(\frac{600.6,5}{100}=39\left(g\right)\)
=> Khối lượng dung môi : \(600-39=561\left(g\right)\)
Ở 200C cứ 561g H2O hoà tan được 39g KClO3
=> Ở 200C 100g H2O hoà tan được 3,95 g KClO3
Khối lượng nước bay hơi là : \(600-413=187\left(g\right)\)
=> Khối lượng nước còn lại : \(561-187=374\left(g\right)\)
Ở 200C 100g H2O hoà tan được 3,95 g KClO3
=> Ở 200C 374 g H2O hoà tan được 26 g KClO3
=> Khối lượng chất rắn kết tinh : \(39-26=13\left(g\right)\)

Khối lượng Kali clorat (KClO3) tại 20 độ C = (600 x 6,5) / 100 = 39g
Như vậy, khối lượng dung môi = 600 - 39 = 561g
Cứ 561g nước hòa tan tối đa 39g KClO3, vậy 100g nước hòa tan được tối đa: 39*100/561 = 6,95g KClO3.
Nước bị bay hơi, nhưng KClO3 được giữ lại, do vậy khối lượng H20 đã bay hơi = 600 - 413 = 187g
Vậy, khối lượng nước còn lại = 561 - 187 = 374g
100g nước hòa tan 6,95g KClO3, vậy 374g H2O hòa tan được 26g KClO3 (quy tắc tăng suất)
Do đó, khối lượng chất rắn kết tinh = 39 - 26 = 13g!

/ nồng độ dung dịch KAl(SO4)2 bão hòa ở 20 độ C là 5,66%=> 600g dd KAl(SO4)2 chứa 600*5,66%=33,96g KAl(SO4)2 và 600-33,96g=566,04g H2O
độ tan = (33,96*100)/566,04=5,9996
b/ mH2O còn lại = 566,04-200=366,04g
nKAl(SO4)2=33,96/258 (mol)
nH2O=336,04/18(mol)
KAl(SO4)2 + 12H2O --->KAl(SO4)2.12H2O
33,96/258--------336,04/18
=> H2O dư
=>nKAl(SO4)2.12H2O=nKAl(SO4)2=33,96/25...
=>mKAl(SO4)2.12H2O=33,96/258*474=62,39...

Đáp án D
Trong 140 gam dung dịch KClO3 bão hòa ở 80°C có 40 gam KClO3. Nên trong 350 gam dung dịch KClO3 bão hào ở 80°C có 100 gam KClO3.
Trong 108 gam dung dịch KClO3 bão hòa ở 20°C có 8 gam KClO3. Gọi số gam KClO3 tách ra khỏi dung dịch là a. Khi đó khối lượng dung dịch và khối lượng KClO3 trong dung dịch thu được lần lượt là 350 – a và 100 – a (gam).
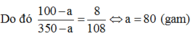

Còn gì nữa ko bài này chỉ xem thôi ko cần tính cái gì à

Câu 1 :
Ta có : \(20\%=\dfrac{m_{ct}}{m_{dd}}.100\%\left(I\right)\)
Mà : \(25\%=\dfrac{m_{ct}}{m_{dd}-75}.100\%\left(II\right)\)
- Giair hệ phương trình ( I ) và ( II ) ta được : \(m_{dd}=375\left(g\right)\)


