Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Gọi CTPT của A là CxHyOz.
Ta có: \(x:y:z=\dfrac{40}{12}:\dfrac{6,67}{1}:\dfrac{53,33}{16}=1:2:1\)
⇒ CTĐGN của A là: (CH2O)n.
Mà: MA = 60 (g/mol)
\(\Rightarrow n=\dfrac{60}{12+2+16}=2\)
Vậy: A là C2H4O.
b, CTCT: CH3 - CHO.
Bạn tham khảo nhé!

Đáp án A
Thành phần % khối lượng của O = 100 – (52,17 + 13,04) = 34,79%
nC : nH : nO = 52,17/12 : 13,04 : 34,79/16 = 4,35 : 13,04 : 2,17 = 2: 6: 1
=> Công thức đơn giản nhất là C 2 H 6 O 2 .
M = (2x12+6+16)n = 46 => n =1
Vậy công thức phân tử: C 2 H 6 O 2

Đặt CTPT của chất là CxHyNz
=> \(x:y:z=\dfrac{\%C}{M_C}:\dfrac{\%H}{M_H}:\dfrac{\%N}{M_N}=\dfrac{70,59}{12}:\dfrac{12,94}{1}:\dfrac{16,47}{14}=5:11:1\)
=> CTĐGN của X là \(\left(C_5H_{11}N\right)_n\)
=> \(n=\dfrac{85}{85}=1\left(TM\right)\)
=> X là C5H11N

%O=100−(65,92+7,75)=26,33%
ta có :x:y:z=\(\dfrac{65,92}{12}=\dfrac{7,75}{1}=\dfrac{26,33}{16}\)
=>x:y:z=10:14:3
=>công thức làC10H14O3

\(M_Z=\dfrac{5,05}{0,1}=50,5\left(g/mol\right)\)
\(m_{Cl}=\dfrac{50,5.70,3}{100}=35,5\left(g\right)\Rightarrow n_{Cl}=\dfrac{35,5}{35,5}=1\left(mol\right)\)
\(m_H=\dfrac{50,5.5,94}{100}=3\left(g\right)\Rightarrow n_H=\dfrac{3}{1}=3\left(mol\right)\)
\(m_C=50,5-35,5-3=12\left(g\right)\Rightarrow n_C=\dfrac{12}{12}=1\left(mol\right)\)
=> CTPT: CH3Cl
CTCT:


- gọi CTTQ của hợp chất hữu cơ là CxHyOz
- %O = 100% - 40% - 6,67% = 53,33 %
MCxHyOz = 30. 2 = 60 (dvc)
- ta có :
+ 12x = \(\dfrac{40}{100}.60\) = 24 => x = 2
+ y = \(\dfrac{6,67}{100}.60\) = 4
+ 16z = \(\dfrac{53,33}{100}.60\) = 32 => z = 2
tỉ lệ :
x:y:z = 2:4:2 = 1:2:1
vậy CTPT của hợp chất hữu cơ là CH2O
Công thức CH2O là công thức đơn giản nhất.
CTPT là (CH2O)n
Ta có : \(n=\dfrac{60}{M_{CH2O}}=\dfrac{60}{30}=2\)
CTPT là: C2H4O2

3. Đốt cháy hoàn toàn 5,75 gam hợp chất hữu cơ X (chứa C, H, O) thu được 11,0 gam CO và 6,75 gam H2O.
a) Tính thành phần phần trăm của các nguyên tố trong X.
b) Lập công thức đơn giản nhất của X.
c) Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với khí hiđro bằng 23
------------------------------------------------------------------
\(a,n_{CO_2}=\frac{11}{44}=0,25mol\)
\(n_{H_2O}=\frac{6,75}{18}=0,375mol\)
Bảo toàn khối lượng ta có:
\(m_{O_2}=12g\Rightarrow n_{O_2}=0,375mol\)
Bảo toàn \(O\)
\(n_O\) trong \(X=0,125mol\)
\(\%m_C=0,25.\frac{12}{5,75}.100\%=52,17\%\)
\(\%m_H=\frac{0,75}{5,75}.100\%=13,04\%\)
\(\%m_O=34,79\%\)
\(n_C:n_H:n_O=0,25:0,75:0,125=2:6:1\)
\(\Rightarrow CT\) đơn giản nhất là \(C_2H_6O\)\(M_X=23.2=46\)
Ta có \(:46n=46\Rightarrow n=1\)
Vậy \(CTPT\) của \(X\) là \(C_2H_6O\)
1. Phân tích một hợp chất hữu cơ thấy: Cứ 2,1 phần khối lượng cacbon lại có 2,8 phần khối lượng oxi và 0,35 phần khối lượng hidro. Hãy xác định công thức phân tử chất hữu cơ, biết rằng 1g chất hữu cơ đó ở (đktc) chiếm thể tích 373,3cm3.
_____________________________
Giải
Ta có :
\(C:H:O=\frac{2,1}{12}:\frac{0,35}{1}:\frac{2,8}{16}\)
\(\rightarrow0,175:0,35:0,175\)
\(=1:2:1\)
\(M=\frac{1}{0,3733:22,4}=60\)
\(\rightarrow CTPT:C_2H_4O_2\)

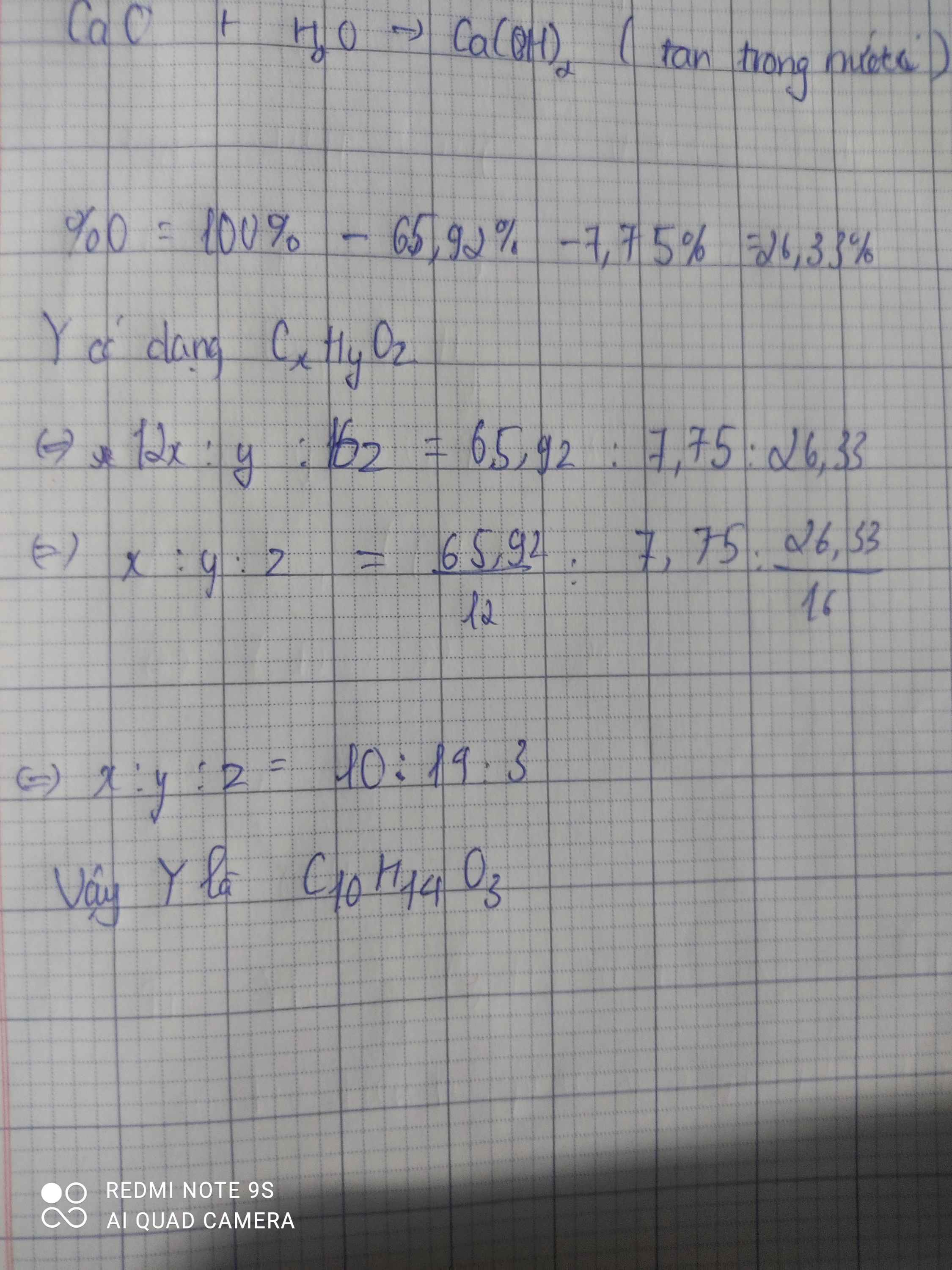
Gọi CTPT của X là CxHyOz.
\(\Rightarrow x:y:z=\dfrac{40}{12}:\dfrac{6,67}{1}:\dfrac{53,33}{16}=1:2:1\)
→ CTPT của X có dạng (CH2O)n.
Mà: X có 2 nguyên tử O. ⇒ n = 2
Vậy: CTPT của X là C2H4O2.
Chất hữu cơ X có phần trăm khối lượng C, H, O lần lượt bằng 40%; 6,67%; 53,33%. Biết trong X có 2 nguyên tử oxi. Công thức phân tử của X?
Ta thấy %C + %H + %O = 100%
=> Hợp chất hữu cơ X chứa 3 nguyên tố C, H, O
Gọi công thức đơn giản nhất của X là CxHyOz
x : y : z = %�12:%�1:%�16=4012:6,671:53,3316=3,33:6,67:3,33=1:2:112%C:1%H:16%O=1240:16,67:1653,33=3,33:6,67:3,33=1:2:1
=> Công thức đơn giản nhất của X là CH2O
Mặt khác trong X có chứa 2 nguyên tử O
=> Công thức phân tử của X sẽ là C2H4O2