Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Sản phẩm cuối cùng sẽ chỉ có Fe2O3, bảo toàn Fe
=> n Fe2O3 = 0,45=> m = 72 gam
=> Đáp án D

Đặt nFe3O4=a
Dung dịch X gồm a mol CuCl2 và 3a mol FeCl2 Fe3O4+8HCl --> FeCl2 + 2FeCl3+4H2O
Cu+ 2Fe3+ --> Cu2+ + 2Fe2+
mX=135a+127.3a=61,92g
=> a=0,12 Đặt nHNO3 dư = x
Dung dịch Y gồm 0,12 mol Cu(NO3)2 , 0,36 mol Fe(NO3)3 và x mol HNO3 (dư)
nNaOH dư = 1,5 - (0,12.2+0,36.3+x)=0,18-x
nNaNO3 = nNaOH pư = 1,5-(0,18-x) = 1,32+x
Hỗn hợp rắn sau nung gồm 1,32+x mol NaNO2 và 0,18-x mol NaOH
m rắn = 40(0,18-x)+69(1,32+x)=100,6
=> x= 0,08
Hỗn hợp khí thoát ra gồm có NO và NO2
Đặt nNO = a, nNO2 =b
Bảo toàn nguyên tố N : a+b=1,6-0,08-0,12.2-0,36.3=0,2
Bảo toàn e : 3a+b=0,12.2+0,12=0,36
=> a=0,08 , b=0,12
Bảo toàn khối lượng : mddY = mCu+mFe3O4+mddHNO3-m khí = 307,6 g
C%Fe(NO3)3= 0,36.242/307,6=28,32%
=> Đáp án B

Đáp án : D
Hỗn hợp 2 khí gồm CO2 và NO2 ( MZ = 45,858g) ( S -> SO4)
nKOH = 1,6 mol
nkết tủa = nBaSO4 = 0,15 mol = nS
C + 4HNO3 -> CO2 + 2H2O + 4NO2
.x -> x -> 4x
S + 6HNO3 -> H2SO4 + 6NO2 + 2H2O
0,15 -> 0,9
=> áp dụng qui tắc đường chéo : nNO2 : nCO2 = 929/71 = (0,9 + 4x) / x
=> x = 0,1 mol
=> m = mC + mS = 6g
2NO2 + 2KOH -> KNO2 + KNO3 + H2O
1,3 -> 1,3 mol
2KOH + CO2 -> K2CO3 + H2O
0,2 <- 0,1
Chất tan gồm 0,1 mol K2CO3 ; 0,65 mol KNO2 ; 0,65 mol KNO3 ; 0,1 mol KOH
=> m1 = 140,3g
=> m + m1 = 146,3g

Đáp án C
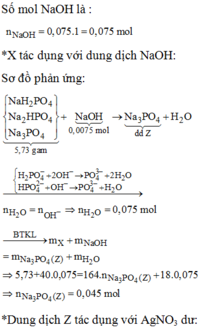
Cho 5,73 gam X tác dụng với 0,075 mol NaOH sẽ thu được dung dịch Z chứa Na3PO4.
BTKL: m N a 3 P O 4 = 5 , 73 + 0 , 075 . 40 - 0 , 075 . 18 = 7 , 38 g a m → n N a 3 P O 4 = 0 , 045 m o l
Cho Z tác dụng với AgNO3 dư thu được kết tủa là 0,045 mol Ag3PO4.
m A g 3 P O 4 = 18 , 855 g a m

Đáp án C

- Giả sử Mg, Fe đều phản ứng hết với muối kim loại => Z chứa toàn bộ số mol Mg2+ ; Fex+
=> T chứa Mg(OH)2 và Fe(OH)x => Chất rắn cuối cùng là MgO và Fe2O3 chắc chắn phải có khối lượng lớn hơn lượng kim loại ban đầu trong X => Không thỏa mãn đề bài (7,2 < 7,36)
=> Các muối nitrat phản ứng hết, kim loại dư và đó là Fe (vì Mg phản ứng trước)
=> kết tủa Y gồm Cu, Ag, Fe.
- Gọi nMg = a ; nFe(pứ) = b ; nFe dư = c => mX = 24a + 56b + 56c = 7,36 (1)
- Bảo toàn e cho phản ứng trao đổi muối: 2nMg + 2nFe pứ = nAg + 2nCu = 2a + 2b
- Khi Y + H2SO4 đặc nóng (Fe → Fe3+)
Bảo toàn electron: 2nCu + nAg + 3nFe dư = 2nSO2 = 2.5,04/22,4 = 0,45 mol
=> 2a + 2b + 3c = 0,45 (2)
- Như đã phân tích ở trên. chất rắn cuối cùng gồm MgO và Fe2O3.
Bảo toàn nguyên tố: nMg = nMgO = a ; nFe2O3 = ½ nFe pứ = 0,5b
=> mrắn = mMgO + mFe2O3 = 40a + 160.0,5b = 40a + 80b = 7,2 (3)
Từ (1,2,3) => a = 0,12 ; b = 0,03 ; c = 0,05 mol
=> mFe(X) = 56.(0,03 + 0,05) = 4,48g
=> %mFe(X) = 4,48: 7,36 = 60,87%



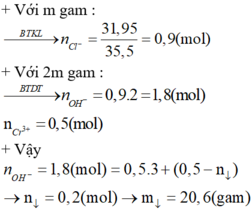
Đáp án B