Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(n_S=\dfrac{6,4}{32}=0,2mol\)
\(Fe+S\rightarrow FeS\)
0,3 0,2 0,2
Sau phản ứng Fe dư và dư 0,1mol.
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
0,2 0,2
\(Fe_{dư}+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,1 0,1
\(\Sigma n_{khí}=0,2+0,1=0,3mol\)
\(\Rightarrow V_{khí}=0,3\cdot22,4=6,72l\)

a.\(Fe+S\rightarrow\left(t^o\right)FeS\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
b.\(n_{hhk}=\dfrac{4,48}{22,4}=0,2mol\)
\(Fe+S\rightarrow\left(t^o\right)FeS\)
Ta thu được hh khí --> S hết, Fe dư
Gọi \(\left\{{}\begin{matrix}n_{Fe}=x\\n_S=y\end{matrix}\right.\)
\(\rightarrow n_{FeS}=n_{Fe}=n_S\rightarrow n_{Fe\left(dư\right)}=x-y\) ( mol )
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(x-y\) \(x-y\) ( mol )
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
y y ( mol )
Ta có: \(\left(x-y\right)+y=0,2\)
\(\Leftrightarrow x=0,2\)
Ta có:\(56x+32y=14,4\)
\(\Leftrightarrow56.0,2+32y=14,4\)
\(\Leftrightarrow y=0,1\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,2.56}{14,4}.100=77,77\%\\\%m_S=100\%-77,77\%=22,23\%\end{matrix}\right.\)

Đáp án B.
nFe = 0,2 mol; nZn = 0,1 mol
NaOH + H2S→NaHS + H2O
![]()

nH2=4,48/22,4=0,2 mol
Fe +2HCl -->FeCl2+H2
0,2 0,2 mol
=>mFe=0,2*56=11,2 g
nSO2=10,08/22,4=0,45 mol
gọi số mol của Cu là a mol
bảo toàn e ta có
Cu\(^0\)-->Cu\(^{+2}\)+2e
a 2a S\(^{+6}\) + 2e -->S\(^{+4}\)
Fe\(^0\)--> Fe\(^{+3}\)+3e 0,45 0,9
0,2 0,6
=>a=0,15=>mCu=0,15*64=9,6 g
=>mhh=9,6+11,2=20,8g
=>%Cu=9,6*100/20,8=46,15%

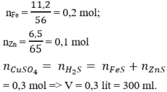


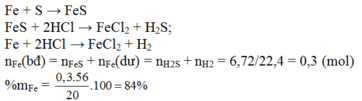
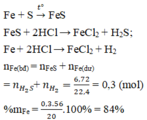




a. ptpư:
Fe + S → FeS
0,2 <----- 0,2 <------ 0,2
FeS + 2HCl → FeCl2 + H2S
0,2 <-------------------------- 0,2
Fe + 2HCl → FeCl2 + H2
0,1 <----------------------- 0,1
H2S + 2NaOH → Na2S + 2H2O
b.
nH2 = 2,24/22,4 = 0,1 mol
nH2S = 6,72/22,4 – 0,1 = 0,2 mol
nFe = 0,3 mol; nS =0,2
mX = (0,2+0,1).56 + 0,2.32 = 23,3 gam