Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
R + HCl → RCl2 + H2
RO + 2HCl → RCl2 + H2O
Ta có: nHCl =0,4.1 = 0,4 mol → ![]() = 0,2 mol →
= 0,2 mol → ![]() = 32
= 32
Theo tính chất của ![]() ta có: M < 32 < M + 16 → 16 < M < 32
ta có: M < 32 < M + 16 → 16 < M < 32
→ M = 24 (Mg) là nghiệm hợp lí

Chọn đáp án D
M + C l 2 → t 0 M C l 2
n M = n M C l 2 ⇒ 7 , 2 M = 28 , 5 M + 71
=> M = 24 (Mg)

Chọn A
Cách 1:
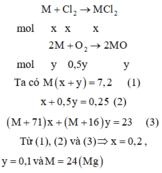
Cách 2:
Gọi số mol của Cl2 và O2 phản ứng lần lượt là x và y mol
→ nkhí = 0,25 mol → x + y = 0,25 (1)
Bảo toàn khối lượng có mkhí= 23 – 7,2= 15,8 gam
→ 71x + 32y = 15,8 (2)
Từ (1) và (2) → x = 0,2 và y = 0,05
Bảo toàn electron có:
2.nM = 2.nCl2 + 4.nO2 → nM= 0,3 → MM = 7,2 : 0,3 = 24 (g/mol)
Vậy kim loại M là Mg.

Bài 1:
Ta có: \(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo ĐLBT KL, có: mM + mCl2 = m muối
⇒ mM = 26,7 - 0,3.71 = 5,4 (g)
PT: \(2M+3Cl_2\underrightarrow{t^o}2MCl_3\)
___0,2____0,3 (mol)
\(\Rightarrow M_M=\dfrac{5,4}{0,2}27\left(g/mol\right)\)
Vậy: M là Nhôm (Al).
Bạn tham khảo nhé!
Bài 2:
Ta có: \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
PT: \(2Na+S\underrightarrow{t^o}Na_2S\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,15}{1}\), ta được S dư.
Theo PT: \(n_{Na_2S}=n_{S\left(dư\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow n_{S\left(dư\right)}=0,05\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Na_2S}=0,1.78=7,8\left(g\right)\\m_{S\left(dư\right)}=0,05.32=1,6\left(g\right)\end{matrix}\right.\)
Bạn tham khảo nhé!

ta có :
2Mg+O2-to>2MgO
x--------0,5x
2Zn+O2-to>2ZnO
y-------0,5y
=>\(\left\{{}\begin{matrix}24x+65y=14,58\\0,5x+0,5y=0,15\end{matrix}\right.\)
=>x=0,12 mol ,y=0,18 mol
=>%mMg=\(\dfrac{0,12.24}{14,58}100\)=19,753%
=>%mZn=80,247%
\(n_{O_2}=\dfrac{4,8}{32}=0,15mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Zn}=y\end{matrix}\right.\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
x 1/2 x ( mol )
\(2Zn+O_2\rightarrow\left(t^o\right)2ZnO\)
y 1/2 y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+65y=14,58\\\dfrac{1}{2}x+\dfrac{1}{2}y=0,15\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,12\\y=0,18\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Mg}=0,12.24=2,88g\\m_{Zn}=0,18.65=11,7g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{2,88}{14,58}.100=19,75\%\\\%m_{Zn}=100\%-19,75\%=80,25\%\end{matrix}\right.\)

Đáp án A
mrắn sau − mM = mX ⇒ 71nCl2 + 32nO2 = 23 − 7,2 = 15,8 g (1)
⇒nkhí = nCl2 +nO2 = 0,25 mol (2)
Giải hệ (1) và (2) ⇒nCl2 = 0,2; nO2 = 0,05 mol
Gọi hóa trị của M là x
Bảo toàn e

M = ![]() = 12x, x = 2 => M = 24 (Mg)
= 12x, x = 2 => M = 24 (Mg)

\(\text{Ta có }n_M=\dfrac{10,8}{M_M}\left(mol\right);n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:8M+30HNO_3\rightarrow8M\left(NO_3\right)_3+3N_2O+15H_2O\\ \Rightarrow n_M=\dfrac{8}{3}n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow\dfrac{10,8}{M_M}=0,4\\ \Rightarrow M_M=27\)
Vậy M là nhôm (Al)
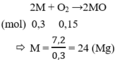
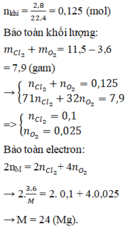
\(n_{Cl_2}=\dfrac{2,7216}{22,4}=0,1215\left(mol\right)\)
PTHH: 2R + 3Cl2 --to--> 2RCl3
___0,081<-0,1215
=> \(M_R=\dfrac{4,212}{0,081}=52\left(g/mol\right)\)
=> R là Cr