Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=a\left(mol\right)\)
\(n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=19.3\left(g\right)\left(1\right)\)
\(n_{H^+}=0.2\cdot2+0.2\cdot2.25\cdot2=1.3\left(mol\right)\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(Fe+2H^+\rightarrow Fe^{2+}+H_2\)
\(n_{H^+}=3a+2b=1.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.2\)
\(\%Al=\dfrac{0.3\cdot27}{19.3}\cdot100\%=41.96\%\)
\(\%Fe=58.04\%\)
\(b.\)
\(n_{H_2}=\dfrac{1}{2}n_{H^+}=0.65\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=19.3+0.4\cdot36.5+0.45\cdot98-0.65\cdot2=76.7\left(g\right)\)

Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,045 0,09 0,045
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
a) Số mol của sắt
nFe = \(\dfrac{0,045.1}{1}=0,045\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,045 . 56
= 2,52 (g)
Khối lượng của bạc
mAg = 4,68 - 2,52
= 2,16 (g)
b) 0/0Fe = \(\dfrac{m_{Fe}.100}{m_{hh}}=\dfrac{2,52.100}{4,68}=\) 53,850/0
0/0Ag = \(\dfrac{m_{Ag}.100}{m_{hh}}=\dfrac{2,16.100}{4,68}=\) 46,150/0
c) Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{0,045.2}{1}=0,09\left(mol\right)\)
Thể tích của dung dịch axit clohidric đã dùng
CM = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}\) = \(\dfrac{0,09}{2}=0,045\left(M\right)\)
Chúc bạn học tốt
Mình xin lỗi bạn nhé , bạn sửa đơn vị của thể tích thành ' lít' giúp mình nhé , tại mình bấm lộn

Ta có nH2 = 3,36/22,4 = 0,15 mol
Fe +2 HCl -> FeCl2 + H2
0,15. 0,3 <-. 0,15. ( Mol)
=> mFe = 0,15 × 56 = 8,4g
=> %Fe = 8,4/15×100% = 56%
=> %Cu = 100% - 56% = 44%
=>VHCl =1\0,3=10\3 l

Bài 1:
\(n_{H_2SO_4}=\dfrac{200.14,7\%}{98}=0,3\left(mol\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\\ m_{Al_2\left(SO_4\right)_3}=342.0,1=34,2\left(g\right)\)
Bài 2:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{Mg}=n_{H_2}=0,15\left(mol\right)\\ \Rightarrow m_{Mg}=0,15.24=3,6\left(g\right)\\ \%m_{Mg}=\dfrac{3,6}{10}.100=36\%\\ \%m_{Cu}=100\%-36\%=64\%\)

a) Gọi $n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 33,4(1)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = 1,5a + b = \dfrac{17,92}{22,4} = 0,8(2)$
Từ (1)(2) suy ra : a = 0,2 ; b = 0,5
$\%m_{Al} = \dfrac{0,2.27}{33,4}.100\% = 16,17\%$
$\%m_{Fe} = 100\% - 16,17\% = 83,83\%$
b) $n_{HCl} = 2n_{H_2} = 1,6(mol)$
c) $m_{muối} = m_{hh} + m_{HCl} - m_{H_2} = 33,4 + 1,6.36,5 - 0,8.2 = 90,2(gam)$

a, Ta có: 65nZn + 27nAl = 11,9 (1)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,1\left(mol\right)\\n_{Al}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ mZn = 0,1.65 = 6,5 (g)
mAl = 0,2.27 = 5,4 (g)
b, Theo PT: nZnCl2 = nZn = 0,1 (mol)
nAlCl3 = nAl = 0,2 (mol)
⇒ m muối = 0,1.136 + 0,2.133,5 = 40,3 (g)
c, Theo PT: nHCl = 2nH2 = 0,8 (mol)
\(\Rightarrow m_{ddHCl}=\dfrac{0,8.36,5}{10\%}=292\left(g\right)\)

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right),n_{Al}=c\left(mol\right)\)
\(m_X=64a+56b+27b=35.7\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{21.84}{22.4}=0.975\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{^{^{t^0}}}CuCl_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(Al+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}AlCl_3\)
\(n_{Cl_2}=a+1.5b+1.5c=0.975\left(mol\right)\left(2\right)\)
\(n_{hh}=ka+kb+kc=0.25\left(mol\right)\)
\(n_{H_2}=kb+k\cdot1.5c=0.2\left(mol\right)\)
\(\Leftrightarrow a-0.25b-0.875c=0\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=0.3,b=0.15,c=0.3\)
\(\%Cu=\dfrac{0.3\cdot64}{35.7}\cdot100\%=53.78\%\)
\(\%Fe=\dfrac{0.15\cdot56}{35.7}\cdot100\%=23.52\%\)
\(\text{%Al=22.7%}\)
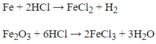
Gọi \(m_{Fe}=x\left(g\right);m_{Al}=y\left(g\right)\) (hiển nhiên \(x,y>0\)), như vậy \(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{x}{56}\left(mol\right)\) và \(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{y}{27}\left(mol\right)\)
Ta ngay lập tức có được \(x+y=16,6\)
Các PTHH xảy ra:
(1) \(Fe+2HCl\rightarrow FeCl_2+H_2\)
(2) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Xét PTHH (1): \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Tỉ lệ mol: 1 : 2 : 1 : 1
Pứ mol: \(\dfrac{x}{56}\) : ? : ? : ?
\(\Rightarrow n_{H_2\left(1\right)}=\dfrac{x}{56}\left(mol\right)\) \(\Rightarrow V_{H_2\left(1\right)}=n_{H_2\left(1\right)}.22,4=\dfrac{x}{56}.22,4=\dfrac{2}{5}x\left(l\right)\) (đktc)
Tương tự ở pthh (2), ta cũng tìm được \(V_{H_2\left(2\right)}=\dfrac{56}{45}y\left(l\right)\)
Như vậy ta có \(\dfrac{2}{5}x+\dfrac{56}{45}y=11,2\) \(\Leftrightarrow18x+56y=504\)
Vậy ta có hpt \(\left\{{}\begin{matrix}x+y=16,6\\18x+56y=504\end{matrix}\right.\), giải hệ này, ta tìm được \(x=11,2;y=5,4\) (nhận)
Vậy khối lượng Fe và Al trong hỗn hợp lần lượt là \(11,2g;5,4g\).