Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{H^+}=2n_{H_2SO_4}+n_{HCl}=2\cdot0,02+0,07=0,11\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,11}{0,35+0,05}=0,275\left(M\right)\) \(\Rightarrow\left[OH^-\right]=\dfrac{10^{-14}}{\left[H^+\right]}\approx3,64\cdot10^{-14}\left(M\right)\)
\(\Rightarrow pH=-log\left(0,275\right)\approx0,56\)
*Môi trường axit và làm quỳ tím hóa đỏ
\(n_{H_2SO_4}=0,05.0,4=0,02\left(mol\right)\\ n_{HCl}=0,2.0,35=0,07\left(mol\right)\\ \left[H^+\right]=\dfrac{0,02.2+0,07}{0,05+0,35}=0,275\left(M\right)\\ pH=-log\left[H^+\right]=-log\left[0,275\right]=0,56\\ \Rightarrow Qùy.hóa.đỏ\)

[H+] = 0,01M = 10-2M => pH = 2
[OH-] = 10-14 / 10-2M =10-12
Dung dịch có pH = 2 < 7 => môi trường axit, quỳ tím có màu đỏ.

[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
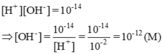
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ

[OH-]=1.10^-14/0.01=10^-12 (M) tính Ph=log[H+] từ kết quả của Ph xem nó lớn hơn 7 hay j xong suy ra môi trường ,môi trường axit thì quỳ đỏ môi trường kiềm quy xanh trung tính ko màu
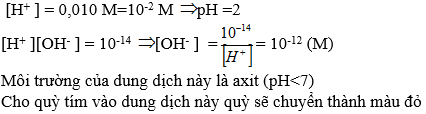
+ \(H_2SO_4\) có \(pH< 7\rightarrow\)Môi trường axit\(\rightarrow\)quỳ hóa đỏ
+ \(KOH\) có \(pH>7\rightarrow\)Môi trường bazo\(\rightarrow\)quỳ hóa xanh
+ \(NaCl\) có \(pH=7\rightarrow\)Môi trường trung tính\(\rightarrow\)quỳ ko đổi
màu
+ \(CH_3COOK\) được tạo từ axit \(CH_3COOH\)(axit mạnh) và bazo KOH(bazo mạnh) có pH>7.Môi trường bazo, quỳ hóa xanh.
+ MgSO4 được tạo từ bazo Mg(OH)2 (bazo yếu) và axit H2SO4 (axit mạnh) có pH<7. Môi trường axit, quỳ hóa đỏ.
+ KF được tạo từ bazo KOH(bazo mạnh) và axit HF( axit yếu) có pH>7. Môi trường bazo, quỳ hóa xanh.