Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tử X có tổng các hạt là 52 : 2Z + N = 52
Số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt : 2Z-N=16
=> \(\left\{{}\begin{matrix}Z=17\\N=18\end{matrix}\right.\)
Vậy: Số P=Số E = Z = 17
Số N = 18

a. Nguyên tử X:
\(\left\{{}\begin{matrix}2P+N=52\\2P-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=17=E=Z\\N=18\end{matrix}\right.\)
Sơ đồ đơn giản:
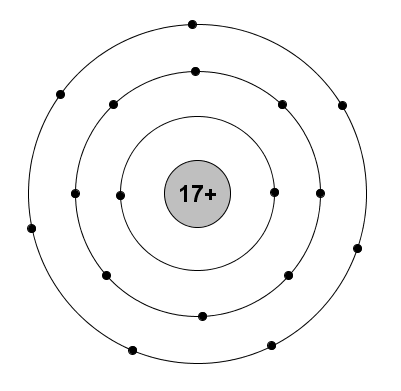
b. * Nguyên tử Y:
\(\left\{{}\begin{matrix}2P+N=28\\N\approx35,7\%.28=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=9\\N=10\end{matrix}\right.\)
Sơ đồ cấu tạo nguyên tử Y:
Em tham khảo nha!

4, a, khối lượng cua 1 nguyen tu Pb la:
207.1,66.10-24= 34,362.10-23 g
b, khối lượng cua 39 nguyen tu Cu la:
39.64.1,66.10-24 = 41,4336.10-22 g
5,a, \(M_A=\dfrac{7,719.10^{-22}}{15.1,66.10^{-24}}=31\)
=> A la P
b, \(M_A=\dfrac{2,13642.10^{-21}}{33.1,66.10^{-24}}=39\)
=> A la K

BÀI 1 :
Gọi số proton,notron,electron của nguyên tử nguyên tố A lần lượt là p,n,e(p,n,eϵN*)
TA CÓ :
p + n + e = 80 => 2p + n = 80 (vì nguyên tử trung hòa về điện) (1)
Do trong nguyên tử nguyên tố A số hạt mang điện lớn hơn số hạt không mang điện là 20 hạt
=> 2p - e = 20
Kết hợp (1) ta được :
2p = 50 => p = 25 (hạt)
=> e = 25 (hạt)
=> n = 30 (hạt)
Vậy số proton , notron , electron của nguyên tử A lần lượt là 25 , 30 , 25 (hạt)
Bài 2 :
Do nguyên tử nguyên tố B có số hạt proton là 17 (hạt)
=> Số electron trong nguyên tử B là 17 (hạt)
TA CÓ :
17 = 2 + 8 + 7
=> Số lớp electron của nguyên tử nguyên tố A là 3 lớp và số electron lớp ngoài cùng là 7 ( hạt )

Theo đề bài ta có: \(\left\{{}\begin{matrix}2Z+N=34\\2Z-N=10\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}Z=11\\N=12\end{matrix}\right.\)
Z=11 => X là Na

1s22s22p63s1
Số e ngoài cùng là 1

1/ta có hệ: \(\begin{cases}2p+n=36\\2p=12\end{cases}\)
<=> p=e=6
n=24
2) ta có hệ : \(\begin{cases}2p+n=52\\n-p=1\end{cases}\)=> p=e=17 , n=18
=> X là Clo (Cl)

cái 17+ là của clo nha

a. Theo đề, ta có HPT:
\(\left\{{}\begin{matrix}2p-n=14\\\dfrac{p}{n}=\dfrac{8}{9}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}\dfrac{2p}{n}-1=\dfrac{14}{n}\\\dfrac{2p}{n}=\dfrac{16}{9}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}1=\dfrac{16}{9}-\dfrac{14}{n}\\2p-n=14\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=18\\p=16\end{matrix}\right.\)
Vậy p = e = 16 hạt, n = 18 hạt.


