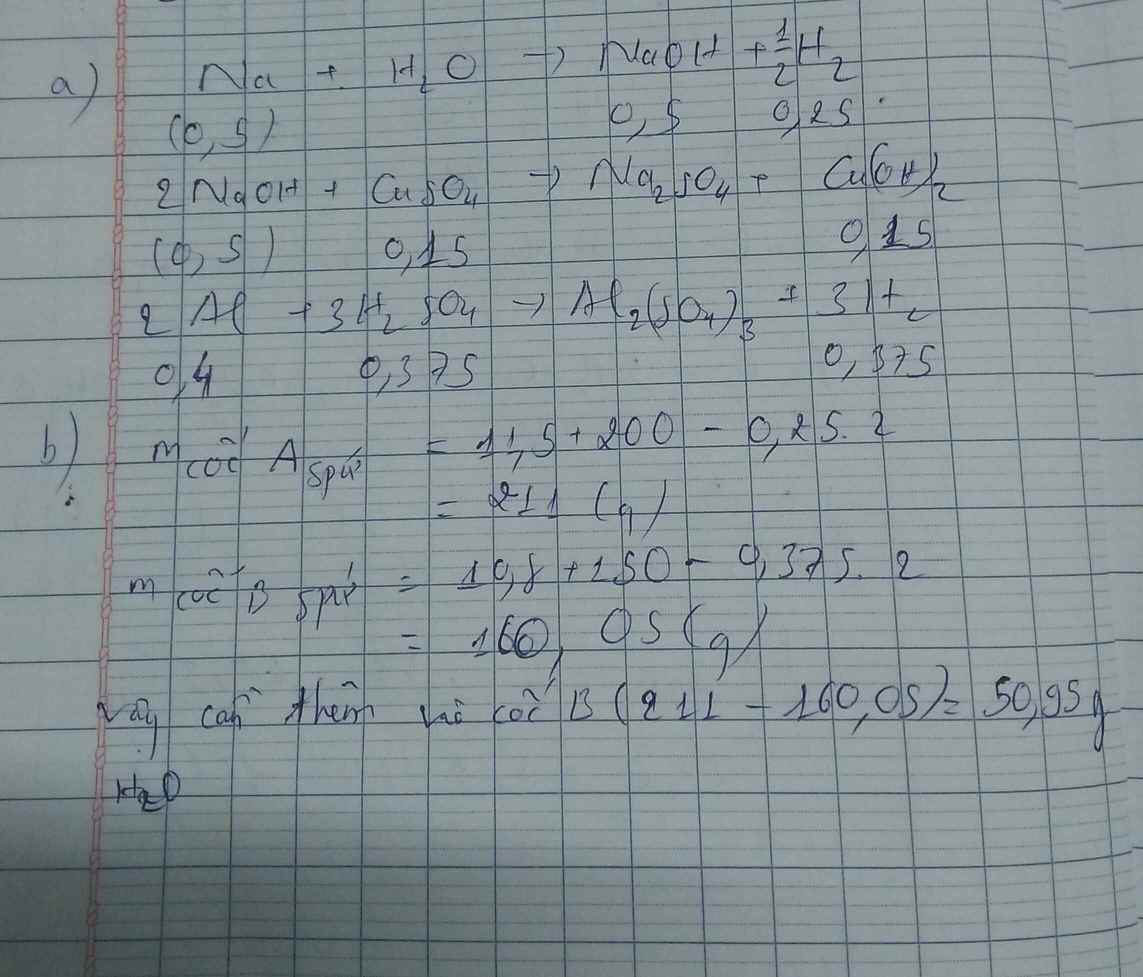Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2. giả sử có 100 g đá vôi
=> mCaCO3=95(g)=>nCaCO3=0,95(mol)
mMgCO3=1,84(g)=>nMgCO3=0,022(mol)
CaCO3 -to-> CaO +CO2(1)
MgCO3 -to-> MgO+CO2(2)
theo (1) : nCO2=nCaCO3=0,95(mol)
theo (2) : nCO2=nMgCO3=0,022(mol)
=>\(\Sigma nCO2=0,972\left(mol\right)\)
=>mCO2=42,768(g)
nếu H=100% thì Hphân hủy =\(\dfrac{40,22}{42,768}.100=94,042\left(\%\right)\)

Giả sử loại đá vôi ban đầu nặng 100g
=> mCaCO3 = 95g ; mMgCO3 =1,28 g ; m tạp chất trơ = 3,72 gam
=> nCaCO3 = \(\dfrac{95}{100}\)=0,95 mol; nMgCO3 = \(\dfrac{1,28}{24}=0,015\left(mol\right)\)mol
Khi nung thì xảy ra phản ứng:
CaCO3 ––(t°)––> CaO + CO2 ↑
MgCO3 ––(t°)––> MgO + CO2 ↑
Ta có: nCO2 = 0,95+0,015=0,965cmol
Nếu đá vôi bị phân hủy hoàn toàn thì khối lượng giảm:
0,965.44=42,46g
Vì khối lượng chất rắn thu được giảm 40,22%
=> m giảm =100.44,22%= 40,22g
Vậy tỉ lệ đá vôi bị phân hủy là \(\dfrac{40,22}{42,46}.100=94,72\%\)

chắc là 4,72g chứ, sao 0,035 mol Ba(OH)2 ra được 4,72kg BaCO3
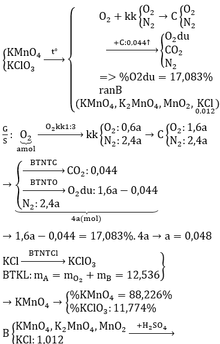
a)
Gọi \(\left\{{}\begin{matrix}n_{KClO_3}=a\left(mol\right)\\n_{KMnO_4}=2a\left(mol\right)\\n_{CaCO_3}=3a\left(mol\right)\end{matrix}\right.\)
=> mA = 122,5a + 316a + 300a = 738,5a (g)
\(\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{122,5a}{738,5a}.100\%=16,588\%\\\%m_{KMnO_4}=\dfrac{316a}{738,5a}.100\%=42,789\%\\\%m_{CaCO_3}=\dfrac{300a}{738,5a}.100\%=40,623\%\end{matrix}\right.\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
a------------>a---->1,5a
2KMnO4 --to--> K2MnO4 + MnO2 + O2
2a-------------->a---------->a------->a
CaCO3 --to--> CaO + CO2
3a----------->3a---->3a
B chứa\(\left\{{}\begin{matrix}KCl:a\left(mol\right)\\K_2MnO_4:a\left(mol\right)\\MnO_2:a\left(mol\right)\\CaO:3a\left(mol\right)\end{matrix}\right.\)
=> mB = 74,5a + 197a + 87a + 168a = 526,5a (g)
=> \(\left\{{}\begin{matrix}\%m_{KCl}=\dfrac{74,5a}{526,5a}.100\%=14,15\%\\\%m_{K_2MnO_4}=\dfrac{197a}{526,5a}.100\%=37,417\%\\\%m_{MnO_2}=\dfrac{87a}{526,5a}.100\%=16,524\%\\\%m_{CaO}=\dfrac{168a}{526,5a}.100\%=31,909\%\%\end{matrix}\right.\)
b)
khí C chứa \(\left\{{}\begin{matrix}O_2:2,5a\left(mol\right)\\CO_2:3a\left(mol\right)\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,5.0,07=0,035\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{4,72}{197}\approx0,024\left(mol\right)\)
TH1: Nễu kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,024<--0,024
=> 3a = 0,024
=> a = 0,008
V = (2,5a + 3a).22,4 = 0,9856 (l)
mA = 738,5a = 5,908 (g)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,035--->0,035--->0,035
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,011--->0,011
=> 3a = 0,035 + 0,011
=> a = \(\dfrac{23}{1500}\)
=> V = (2,5a + 3a).22,4 = 1,889 (l)
mA = 738,5a = 11,3237 (g)

a)
$2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
Gọi $n_{CuO} = n_{Cu(NO_3)_2\ pư} = a(mol)$
Suy ra:
$m_{giảm} = 188a - 80a = 54 \Rightarrow a = 0,5(mol)$
$m_{Cu(NO_3)_2\ pư} = 0,5.188 = 94(gam)$
b)
$n_{NO_2} = 4a = 2(mol)$
$n_{O_2} = 0,5a = 0,25(mol)$
$V_{NO_2} = 2.22,4 = 44,8(lít)$
$V_{O_2} = 0,25.22,4 = 5,6(lít)$

b.
4P + 5O2 → 2P2O5
0,16→ 0,2
Dư: 0,025
Sau pứ m(bình 1) = mP2O5 = 11,36 (g)
O2 + 2C → 2CO
0,025→ 0,05 0,05
Dư: 0,25
Sau pứ m(bình 2) = mCdư = 3 (g)

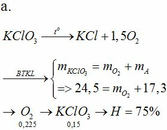
mCaCO3 nguyên chất = 500* 95%=475(g)
=> nCO2 tạo thành= 4.75 mol
sau một thời gian ... => m CO2 thực (ĐLBTKL ) = 167.2 (g)
=> nO2 thực = 3.8 mol
=> H% = 3.8 / 4.75 *100=80%
P/s Trình bày hẳn hoi bạn nhé , mk sơ lược thế thôi .
# Hoc_tot_nhoa#

Phản ứng này không tạo khí bạn nhé :
200ml = 0,2l
300ml = 0,3l
\(n_{MgCl2}=\dfrac{19}{95}=0,2\left(mol\right)\)
a) Pt : \(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl|\)
1 2 1 2
0,2 0,2 0,4
\(n_{Mg\left(OH\right)2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{Mg\left(OH\right)2}=0,2.58=11,6\left(g\right)\)
Pt : \(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O|\)
1 1 1
0,2 0,2
\(n_{MgO}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{MgO}=0,2.40=8\left(g\right)\)
c) \(n_{NaCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
\(V_{ddspu}=0,2+0,3=0,5\left(l\right)\)
\(C_{M_{NaCl}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Chúc bạn học tốt