Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
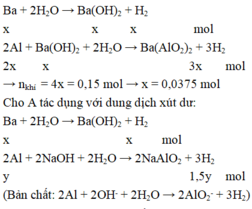

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

Chất không tan là Ag.
=> mAg= 6,25(g)
nH2=0,25(mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
-> nZn=nH2= 0,25(mol)
=>mZn= 0,25 . 65=16,25(g)
=>
%mAg = \(\dfrac{6,25}{6 , 25 + 16 , 25}\) . 100 ≈ 27,778%
⇒% mZn ≈ 72,222%

\(n_{H_2}=0,3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
a---------2a---------------------a
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b---------2b--------------------b
\(\Rightarrow\left\{{}\begin{matrix}24a+65b=15,3\\a+b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,102\\b=0,198\end{matrix}\right.\)
\(m_{Mg}=0,102.24=2,448\left(g\right)\)
\(m_{Zn}=15,3-2,448=12,852\left(g\right)\)
\(n_{HCl}=2.0,102+2.0,198=0,6\left(mol\right)\)
\(V_{HCl}=\dfrac{n}{C_M}=\dfrac{0,6}{1}=0,6\left(l\right)=600\left(ml\right)\)
a) Gọi x, y là số mol Mg, Zn
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(\left\{{}\begin{matrix}24x+65y=15,3\\x+y=0,3\end{matrix}\right.\)
=> \(x=\dfrac{21}{205};y=\dfrac{81}{410}\)
\(\%m_{Mg}=\dfrac{\dfrac{21}{205}.24}{15,3}.100=16,07\%\)
%m Zn = 83,93%
b)Bảo toàn nguyên tố H \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,6}{1}=0,6\left(lít\right)=600ml\)

TN1: A tác dụng với nước
Ba +2 H2O --> Ba(OH)2 + H2;
x ------------------x------------x ;
2Al + Ba(OH)2 +2 H2O --> Ba(AlO2)2 +3 H2;
2x--------x---------------------------------------3x;
TN2 : A tác dụng với dd xút
Ba +2 H2O --> Ba(OH)2 + H2;
x----------------------------------x;
2Al + Ba(OH)2 +2 H2O --> Ba(AlO2)2 +3 H2;
y-------------------------------------------------3/2y;
TN3: A tác dụng với HCl
Ba + 2HCl --> BaCl2 + H2;
x------------------------------x;
2Al + 6HCl --> 2AlCl3 + 3H2;
y------------------------------3/2y;
Mg + 2HCl --> MgCl2 + H2;
z------------------------------z;
Gọi x,y,z lần lượt là số mol của Ba, Al, Mg.
TN1: nH2= 3,36/22,4= 0,15 (mol)
=>x + 3x= 4x=0,15 => x= 0,0375 (mol)
TN2: nH2= 0,3 (mol)
=> x + 3/2 y = 0,3 => y = 0,175 (mol)
TN3: nH2= 0,4 (mol)
=> x +3/2y + z = 0,4 => Z= 0,1 (mol)
m= 0,0375*137+ 0,175*27+ 0,1*24=26,2625(g).

Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : Mg + 2HCl → MgCl2 + H2\(|\)
1 2 1 1
a 0,2 1a
Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
b 0,4 1b
a) Gọi a là số mol của Mg
b là số mol của Zn
Theo đề ta có : mMg + mZn = 15,4 (g)
⇒ nMg . MMg + nZn . MZn = 15,4 g
24a + 65b = 15,4g (1)
Theo phương trình : 1a + 1b = 0,3 (2)
Từ (1),(2), ta có hệ phương trình :
24a + 65b = 15,4
1a + 1b = 0,3
⇒ \(\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
Khối lượng của magie
mMg = nMg . MMg
= 0,1. 24
= 2,4 (g)
Khối lượng của kẽm
mZn = nZn . MZn
= 0,2 . 65
= 13 (g)
b) Số mol tổng của dung dịch axit clohidric
nHCl = 0,2 + 0,4
= 0,6 (mol)
Thể tích của dung dịch axit clohidirc đã dùng
CMHCl = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{0,6}{1}=0,6\left(l\right)\)
Chúc bạn học tốt

\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`

Bài 4:
a) nH2= 6,72/22,4= 0,3(mol)
Đặt:nMg= x(mol); nZn=y(mol) (x,y>0)
PTHH: Mg + 2 HCl -> MgCl2 + H2
x_______2x________x_____x(mol)
Zn + 2 HCl -> ZnCl2 + H2
y____2y____y________y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}24x+65y=15,4\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
mMg=0,1.24=2,4(g)
=>%mMg = (2,4/15,4).100=15,584%
=>%mZn= 84,416%
b) nHCl(tổng)= 0,6(mol)
=> VddHCl=0,6/1=0,6(l)
Chúc em học tốt!
 =)))
=)))
Bài 1:
n H2=5.6/22.4=0.25(mol) ZnSO4 + H2
ZnSO4 + H2
Zn + H2SO4
0.25 0.25
m Zn=0.25*65=16.25(g)
m hh=16.25+6.25=22.5(g)
% Zn=16.25/22.5*100%=72.22%
% Ag=100%-72.22%=27.78%
Bài 2:
nH2 = 6,72/22,4 = 0,3 mol MgCl2 + H2
MgCl2 + H2  ZnCl2 + H2
ZnCl2 + H2
gọi x,y lần lượt là số mol của Mg và Zn tham gia phản ứng.
Mg + 2HCl
x 2x x
Zn + 2HCl
y 2y y
Ta có phương trình
x + y = 0,3
24x + 56y = 15,3
=> x = 0,102 ; y = 0.198
m Mg = 0,102.24 = 2,448 g
m Zn = 0,198.65 = 12.87 g
n HCl = 2.0,102+2.0,198 = 0,6 mol
V HCl = 0,6/1 = 0,6 lít.
Bài 3:
TN1 Ba(OH)2 + H2
Ba(OH)2 + H2
 2NaAlO2 + 3H2
2NaAlO2 + 3H2
 BaCl2 + H2
BaCl2 + H2
 2AlCl3 + 3H2
2AlCl3 + 3H2
 MgCl2 + H2
MgCl2 + H2
n H2=3.36/22.4=0.15(mol)
Ba + 2H2O
0.15 0.15
TN2
n H2 = 6.72/22.4=0.3(mol)
2Al + 2NaOH + 2H2O
0.2 0.3
TN3
n H2=8.96/22.4=0.4(mol)
Ba + 2HCl
0.15 0.15
2Al + 6HCl
0.2 0.2
Mg + 2HCl
0.05 0.05
m Ba=0.15*137=20.55(g)
m Al=0.2*27=5.4(g)
m Mg=0.05*24=1.2(g)
m=20.55+5.4+1.2=27.15
%Ba=20.55/27.15*100%=75.69%
%Al=5.4/27.15*100%=19.89%
%Mg=100%-75.69%-19.89%=4.42%