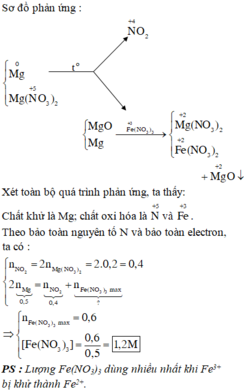
Cho 7,2 gam hỗn hợp X gồm S và Fe vào một bình kín không có oxi. Nung bình cho đến khi phản ứng xảy ra hoàn toàn, thu được chất rắn A. Cho A tác dụng với dung dịch H 2 S O 4 loãng, dư thu được 2,24 lít hỗn hợp khí Y (đktc). Tỉ khối của Y so với H 2 là
A. 17
B. 9
C. 8,5
D. 10



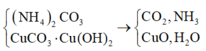

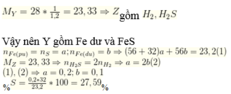
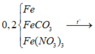
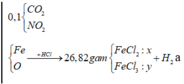
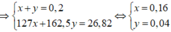

Chọn B