Hòa tan m gam hỗn hợp gồm Cu và F e 3 O 4 trong dung dịch HCl dư sau phản ứng còn lại 8,32gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m là:
A. 31,04 g
B. 40,10 g
C. 43,84 g
D. 46,16 g
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có các phản ứng sau:
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
Cu + 2FeCl3 → CuCl2 + 2FeCl2
Đặt n Fe3O4 = x mol
=> hỗn hợp muối gồm : x mol CuCl2 ; 3x mol FeCl2
Chất rắn còn dư chính là Cu.
=> m muối = 135x+127.3x =61,92 => x = 0,12 mol
=> m= m Fe3O4+ mCu = 232.0,12 + 64.0,12 + 8,32=43,84 g
=> B

Có các phản ứng sau:
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
Cu + 2FeCl3 → CuCl2 + 2FeCl2
Đặt n Fe3O4 = x mol
=> hỗn hợp muối gồm : x mol CuCl2 ; 3x mol FeCl2
Chất rắn còn dư chính là Cu. => m muối = 135x+127.3x =61,92
=> x = 0,12 mol
=> m= m Fe3O4+ mCu = 232.0,12 + 64.0,12 + 8,32=43,84 g => B

Đáp án : D
Do sau phản ứng có chất rắn => Cu dư và sau phản ứng dung dịch có FeCl2 ; CuCl2
Fe3O4 + 8HCl à FeCl2 + 2FeCl3 + 4H2O
x à x à 2x
Cu + 2FeCl3 à CuCl2 + 2FeCl2
x ß 2x à x à 2x
=> m muối = m FeCl2 + m CuCl2 => 61,92g = 3x.127 + x.135 => x = 0,12mol
=> m = mFe3O4 + mCu pứ + mCu dư = 43,86g

Đặt nFe3O4=a
Dung dịch X gồm a mol CuCl2 và 3a mol FeCl2 Fe3O4+8HCl --> FeCl2 + 2FeCl3+4H2O
Cu+ 2Fe3+ --> Cu2+ + 2Fe2+
mX=135a+127.3a=61,92g
=> a=0,12 Đặt nHNO3 dư = x
Dung dịch Y gồm 0,12 mol Cu(NO3)2 , 0,36 mol Fe(NO3)3 và x mol HNO3 (dư)
nNaOH dư = 1,5 - (0,12.2+0,36.3+x)=0,18-x
nNaNO3 = nNaOH pư = 1,5-(0,18-x) = 1,32+x
Hỗn hợp rắn sau nung gồm 1,32+x mol NaNO2 và 0,18-x mol NaOH
m rắn = 40(0,18-x)+69(1,32+x)=100,6
=> x= 0,08
Hỗn hợp khí thoát ra gồm có NO và NO2
Đặt nNO = a, nNO2 =b
Bảo toàn nguyên tố N : a+b=1,6-0,08-0,12.2-0,36.3=0,2
Bảo toàn e : 3a+b=0,12.2+0,12=0,36
=> a=0,08 , b=0,12
Bảo toàn khối lượng : mddY = mCu+mFe3O4+mddHNO3-m khí = 307,6 g
C%Fe(NO3)3= 0,36.242/307,6=28,32%
=> Đáp án B

TN1: Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
2FeCl3 + Cu → CuCl2 + 2FeCl2
Vì Cu còn dư 0,1 mol nên sau phản ứng chứa FeCl2 : 3a mol, CuCl2 : a mol
→ a. 232 + 64. ( a + 0,1)= 24,16 → a = 0,06 mol
Vậy X gồm Cu: 0,16 mol và Fe3O4 : 0,06 mol
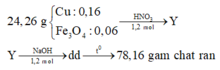
+ Nhận thấy nếu chất rắn chỉ chứa NaNO2 : 0,12 mol thì mchất rắn = 0,12. 69 > 78,16 gam.
⇒ Chất rắn chứa đồng thời NaNO2 : x mol và NaOH : y mol
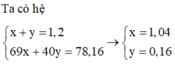
Giả sử sản phẩm khử chứa N và O
Bảo toàn nguyên tố N → nN = 1,2 - 1,04 = 0,16 mol
Bảo toàn electron → 2nCu + nFe3O4 = 5nN - 2nO → nO = 0,21 mol
Bảo toàn khối lượng → mdd = 24,16 + 240 - 0,16.14 - 0,21. 16 = 258,56 gam
%Cu(NO3)2 = 0 , 16 . 188 258 , 56 . 100% = 11,63%.

Chọn đáp án B
TN1: Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
2FeCl3 + Cu → CuCl2 + 2FeCl2
Vì Cu còn dư 0,1 mol nên sau phản ứng chứa FeCl2 : 3a mol, CuCl2 : a mol → a. 232 + 64. ( a + 0,1)= 24,16 → a = 0,06 mol
Vậy X gồm Cu: 0,16 mol và Fe3O4 : 0,06 mol
TN2: 24,26 g
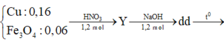
78,16 gam chất rắn
+ Nhận thấy nếu chất rắn chỉ chứa NaNO2 : 0,12 mol thì mchất rắn = 0,12. 69 > 78,16 gam.
⇒ Chất rắn chứa đồng thời NaNO2 : x mol và NaOH : y mol
Ta có hệ
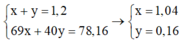
Giả sử sản phẩm khử chứa N và O
Bảo toàn nguyên tố N → nN = 1,2 - 1,04 = 0,16 mol
Bảo toàn electron → 2nCu + nFe3O4 = 5nN - 2nO → nO = 0,21 mol
Bảo toàn khối lượng → mdd = 24,16 + 240 - 0,16.14 - 0,21. 16 = 258,56 gam
%Cu(NO3)2 = 0 , 16 . 188 258 . 56 . 100% = 11,63%. ⇒ Chọn B

Chọn B
Cho hỗn hợp chất rắn phản ứng với HCl dư có Cu không phản ứng.
Phương trình hóa học:
F e + 2 H C l → F e C l 2 + H 2 F e O + 2 H C l → F e C l 2 + H 2 O


Chất rắn D là Cu, chất rắn E là CuO
\(m_{tăng}=m_{O_2}=0,16\left(g\right)\)
=> \(n_{O_2}=\dfrac{0,16}{32}=0,005\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
0,01<-0,005
=> mCu = 0,01.64 = 0,64 (g)
Gọi số mol K, Ba là a, b (mol)
=> 39a + 137b = 3,18 - 0,64 = 2,54 (1)
PTHH: 2K + 2H2O --> 2KOH + H2
a--------------->a
Ba + 2H2O --> Ba(OH)2 + H2
b--------------->b
=> 56a + 171b = 3,39 (2)
(1)(2) => a = 0,03 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,64}{3,18}.100\%=20,126\%\\\%m_K=\dfrac{0,03.,39}{3,18}.100\%=36,792\%\\\%m_{Ba}=\dfrac{0,01.137}{3,18}.100\%=43,082\%\end{matrix}\right.\)
\(m_{O_2}=m+0,16-m=0,16\left(g\right)\\ \rightarrow n_{O_2}=\dfrac{0,16}{32}=0,005\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
0,01 0,005
Gọi \(\left\{{}\begin{matrix}n_K=a\left(mol\right)\\n_{Ba}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
2K + 2H2O ---> 2KOH + H2
a a
Ba + 2H2O ---> Ba(OH)2 + H2
b b
Hệ pt \(\left\{{}\begin{matrix}39a+137b=3,18-0,01.64=2,54\\56a+171b=3,39\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,03\left(mol\right)\\b=0,01\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,01.64}{3,18}=20,13\%\\\%m_K=\dfrac{0,03.39}{3,18}=36,79\%\\\%m_{Ba}=100\%-20,13\%-36,79\%=43,08\%\end{matrix}\right.\)
Ta thấy sau phản ứng còn Cu dư, chứng tỏ F e 3 O 4 tác dụng với HCl tạo 2 muối F e C l 3 và F e C l 2 , sau đó F e C l 3 tác dụng hết với Cu tạo F e C l 2 và . C u C l 2
PTHH:
F e 3 O 4 + 8 H C l → 2 F e C l 3 + F e C l 2 + 4 H 2 O
x…………………....2x………x
2 F e C l 3 + C u → 2 F e C l 2 + C u C l 2
2x……..x…………2x………..x
m m u o i = m F e C l + m C u C l 2
= (2x+x).127 + x.135 = 61,92g
⇒ x= 0,12 mol
⇒ m h h b a n d a u = m F e 3 O 4 + m C u p ư + m C u d ư
= 0,12.232+ 0,12.64+ 8,32= 43,84g
⇒ Chọn C.