Cho hỗn hợp (N, Al) lấy dư vào 91,6 g dung dịch H2SO4 21,4% thu được V lít khí H2 ở đktc. Tính V ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Fe}=a\left(mol\right),n_{FeO}=b\left(mol\right)\)
\(m_X=56a+72b=12.8\left(g\right)\)
\(n_{H_2}=n_{Fe}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\Rightarrow a=0.1\)
\(b=\dfrac{12.8-56\cdot0.1}{72}=0.1\left(mol\right)\)
\(BTe:\)
\(3n_{Fe}+n_{FeO}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=\dfrac{3\cdot0.1+0.1}{2}=0.2\left(mol\right)\)
\(V_{SO_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(\)

PTHH: \(Fe+H_2SO_{4\left(l\right)}\rightarrow FeSO_4+H_2\uparrow\)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=n_{H_2}=0,1\left(mol\right)\\n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{Cu}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Cu}+m_{Fe}=0,1\cdot56+0,05\cdot64=8,8\left(g\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
_ Khi pư với H2SO4 loãng.
Theo ĐLBT mol e, có: 2y = 0,1.2 ⇒ y = 0,1 (mol) (1)
_ Khi pư với H2SO4 đặc nóng.
Ta có: \(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo ĐLBT mol e, có: 2x + 3y = 0,2.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
⇒ m = mCu + mFe = 0,05.64 + 0,1.56 = 8,8 (g)
Bạn tham khảo nhé!

Chọn C
Gọi số mol Na, Al và Fe có trong m gam G lần lượt là x, y và z (mol)
Do khi cho G vào nước thu được số mol khí ít hơn khi cho G vào NaOH dư nên khi cho G vào nước dư chỉ có Na phản ứng hết.


\(n_{H^+}=0,5.0,8+0,25.0,8.2=0,8\left(mol\right)\\ \Rightarrow n_{H_2}=\dfrac{n_{H^+}}{2}=\dfrac{0,8}{2}=0,4\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,4.22,4=8,96\left(l\right)\)
Không phải KL hhX cho rồi à ta?

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
0,2 0,3
\(\rightarrow m_{Al}=0,2.27=5,4\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{5,4}{13,4}=40,3\%\\\%m_{CuO}=100\%-40,3\%=59,7\%\end{matrix}\right.\\ n_{CuO}=\dfrac{13,4-5,4}{80}=0,1\left(mol\right)\)
PTHH:
2Al + 6H2SO4 ---> Al2(SO4)3 + 3SO2 + 6H2O
0,2 0,6 0,1 0,3
CuO + H2SO4 ---> CuSO4 + H2O
0,1 0,1 0,1
\(V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Mặc định C% H2SO4 là 98% nhé
\(m_{ddH_2SO_4}=\dfrac{98.\left(0,1+0,6\right)}{98\%}=70\left(g\right)\\ m_{dd\left(sau.pư\right)}=70-64.0,3+13,4=64,2\left(g\right)\)
\(\rightarrow\left\{{}\begin{matrix}C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1.342}{64,2}=53,27\%\\C\%_{CuSO_4}=\dfrac{0,1.160}{64,2}=24,92\%\end{matrix}\right.\)
a)\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(m_{Al}=0,2\cdot27=5,4g\)
\(\%m_{Al}=\dfrac{5,4}{13,4}\cdot1005=40,3\%\Rightarrow\%m_{CuO}=59,7\%\)
Câu b có thiếu dữ kiện đề bài không nhỉ

Chọn C
Gọi số mol của Fe và Al lần lượt là x và y mol

Muối trong dung dịch A gồm x mol F e S O 4 và 0,5y mol A l 2 ( S O 4 ) 3


Giải thích:
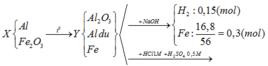
BT e: nAl dư = 2/3 nH2 = 2/3. 0,15 = 0,1 (mol)
BTNT: Fe => nFe2O3 = ½ nFe = 0,15 (mol)
Phản ứng xảy ra hoàn toàn, Al dư sau phản ứng ( vì Y + NaOH có khí H2 bay ra), do đó Fe2O3 phản ứng hết
Fe2O3 + 2Al Al2O3 + 2Fe
0,15 → 0,3
=> nAl ban đầu = 0,3 + 0,1 = 0,4 (mol)
nHCl = V (mol) ; nH2SO4 = 0,5V (mol)
Bảo toàn điện tích khi cho Y tác dụng với hh axit
=> 2nFe2+ + 3nAl3+ = nCl- + 2nSO42-
=> 2.0,3 + 3. 0,4 = V + 2. 0,5V
=> V = 0,9 (lít)
Đáp án B
