Trình bày cách phân biệt bột giấy với bột cát!
Hóa học lớp 8.
Giúp mình gấp với ạ!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 1:
- Đổ dd vào các chất rồi khuấy đều, sau đó nhúng quỳ tím
+) Tan và làm quỳ tím hóa đỏ: P2O5
+) Tan, dd vẩn đục và làm quỳ tím hóa xanh: CaO
+) Không tan: MgO
Bài 3:
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
a_______a________a_____a (mol)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
b_______b_______b_____b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}24a+56=8\\a+b=\dfrac{4,48}{22,4}=0,2\end{matrix}\right.\) \(\Leftrightarrow a=b=0,1\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{24\cdot0,1}{8}\cdot100\%=30\%\\\%m_{Fe}=70\%\\C_{M_{H_2SO_4}}=\dfrac{0,1+0,1}{0,5}=0,4\left(M\right)\end{matrix}\right.\)

Thả vào nước và cho thử QT:
- Tan, chuyển xanh -> Na2O
- Tan, QT chuyển đỏ -> P2O5
- Ko tan -> Fe2O3
- Tan ít, QT chuyển xanh -> CaO

Trích mỗi chất 1 ít dung dịch để làm mẫu thử và cho vào ống nghiệm
B1:Dùng quỳ tím làm mẫu thử:chất nào hóa màu hồng(đỏ) thì đó là axit axetic
B2:Lấy Na là mẫu thử:mẫu nào có khí ko màu thoát ra thì đó là rượu etylic
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\uparrow\)
B3:Ta lấy Bạc oxit(\(Ag_2O\) ) làm mẫu thử,chất nào có kết tủa trắng thì đó là dd glucozo
\(C_6H_{12}O_6+Ag_2O\xrightarrow[NH_3]{t^o}C_2H_{12}O_7+2Ag\downarrow\)
B4:Ta cho hồ tinh bột tác dụng với dung dịch Iot(\(I_2\) )thì dung dịch sẽ chuyển màu xanh tím
Chất còn lại là benzen

Trích mẫu thử:
Cho nước lần lượt vào từng mẫu thử :
- Tan , tạo thành dung dịch : Na2O , P2O5 , BaCl2 , Na2CO3 (1)
- Không tan : CaCO3 , MgO (2)
Cho quỳ tím vào các dung dịch thu được ở (1) :
- Hóa xanh : Na2O
- Hóa đỏ : P2O5
Cho dung dịch HCl vào các chất còn lại ở (1) :
- Sủi bọt khí : Na2CO3
- Không HT : BaCl2
Cho dung dịch HCl vào các chất ở (2) :
- Tan , sủi bọt : CaCO3
- Tan , tạo dung dịch : MgO
PTHH em tự viết nhé !
Trích mẫu thử.
Cho nước vào từng mẫu thử:
- Không tan: CaCO3, MgO
- Tan: Na2O, P2O5, BaCl2, Na2CO3 (*)
Cho giấy quỳ vào dd ở (*):
- Quỳ hóa đỏ: P2O5 \(\left(P_2O_5+3H_2O\rightarrow2H_3PO_4\right)\) (**)
- Quỳ hóa xanh: Na2O \(\left(Na_2O+H_2O\rightarrow2NaOH\right)\)
- Quỳ không đổi màu: BaCl2, Na2CO3 (***)
Đưa dd thu được ở (**) vào 2 dd ở (***)
- Không tác dụng: BaCl2
- Tác dụng, tạo chất khí và muối: Na2CO3 \(\left(Na_2CO_3+H_3PO_4\rightarrow Na_3PO_4+H_2O+CO_2\right)\)

Saccarozơ, andehit axetic, hồ tinh bột
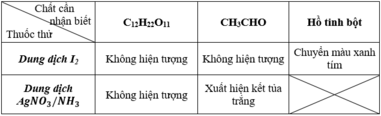
Trích mẫu thử, chọn thuốc thử: I2 và dd AgNO3/NH3
Hiện tượng
Cho I2 vào 3 mẫu thử, mẫu thử nào dung dịch chuyển sang màu xanh tím là hồ tinh bột.
Cho dung dịch AgNO3/NH3 vào hai mẫu thử còn lại mẫu thử nào có kết tủa trắng là andehit axetic
PTHH:
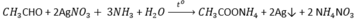

Hòa tan vào nước nhg~ gói tan là bột gạo,bột đá vôi,bột cát trắng,bột giấy;nhg~ góitan tốt tạo thành dung dịnh trong suốt là xoda,muối ăn. còn vôi sống tan một phần; phần còn lại đục ngầu. pu tỏa nhiệt dd nhờn, cho quỳ tím vào thì quỳ chuyển màu xanh
CaO + H20 ->Ca(OH)2 tan it'
CHo HCL vào dd soda và muối ăn nếu có khí thoát ra là soda còn lại là muối ăn
Na2CO3 + HCl ===) NaCL + H2O + C02
CHo dd Hcl vào các gói ko tan trong nước nếu thấy sủi bọt khí lad đá vôi
CaCO3 + HCL -> CaCl2 + H2O + Co2
CHo một ít nước vào 3 gói còn lại đun nóng nhẹ rồi lại cho dd I2 vào nếu thấy dd có màu xanh xuất hiện là tinh bột
Để phân biệt bột cát và bột giấy ta đốt cháy SiO2 ko cháy cong giấy cháy thành Co2 và H20
(C6H10O5)n + O2 -> CO2 + H2O

Khả năng để một hợp chất hòa tan được trong một hợp chất khác được gọi là tính tan. Khi một chất lỏng có thể hòa tan hoàn toàn vào một chất lỏng khác thì hai chất lỏng đó có thể trộn lẫn vào nhau được. Hai chất mà không thể trộn với nhau để tạo thành dung dịch thì được gọi là không trộn lẫn vào nhau được.
Tất cả các dung dịch đều có entropy rõ ràng khi trộn lẫn. Sự tương tác giữa các phân tử hoặc ion khác nhau có thể thuận lợi về mặt năng lượng hoặc không. Nếu sự tương tác không thuận lợi, thì năng lượng tự do sẽ giảm đi khi nồng độ chất tan ngày càng tăng. Vào một thời điểm nào đó phần năng lượng mất đi sẽ cao hơn là entropy có được, và không có các cấu tử chất tan nào có thể được hòa tan nữa; khi đó dung dịch được cho là bão hòa. Tuy nhiên, thời điểm mà một dung dịch có thể trở thành bão hòa có thể thay đổi đáng kể với các nhân tố môi trường khác nhau, chẳng hạn như nhiệt độ, áp suất và sự ô nhiễm. Với vài sự kết hợp giữa dung môi và chất tan thì một dung dịch siêu bão hòa có thể được tạo ra bằng cách tăng khả năng hòa tan (ví dụ bằng cách tăng nhiệt độ) để hòa tan chất tan nhiều hơn, và sau đó giảm nó xuống (ví dụ bằng cách làm lạnh). Thường thì khi nhiệt độ dung môi càng cao, các chất tan dạng rắn càng tan nhiều hơn. Tuy nhiên, hầu hết các loại khí và một vài hợp chất lại có tính tan giảm khi nhiệt độ tăng. Đây là do kết quả củaentanpi tỏa nhiệt của dung dịch. Vài hoạt chất bề mặt có tính chất này. Tính tan của chất lỏng trong chất lỏng thì ít thay đổi với nhiệt hơn là chất rắn hay chất khí.
Tính chất[sửa | sửa mã nguồn]
Tính chất vật lý của các hợp chất như điểm chảy và điểm sôi sẽ thay đổi khi các hợp chất khác được thêm vào. Chúng được gọi là những tính chất tập hợp. Có vài cách để định lượng được lượng chất hòa tan trong các hợp chất khác và được gọi chung là nồng độ. Ví dụ như phân tử gam, phần thể tích, và phần mol.
Các tính chất của các dung dịch lý tưởng có thể được tính bằng tổ hợp tuyến tính của những tính chất từ những thành phần của nó. Nếu cả chất tan và dung môi tồn tại với lượng bằng nhau (chẳng hạn như trong một dung dịch gồm 50% êtanol, 50% nước), thì các khái niệm về "chất tan" và "dung môi" trở nên ít liên quan, nhưng chất mà thường được sử dụng như một dung môi thì vẫn thường được xem như là dung môi (trong ví dụ này là nước).
Chất lỏng[sửa | sửa mã nguồn]
Về nguyên tắc, tất cả các loại chất lỏng có thể hoạt động như dung môi: khí hiếm dạng lỏng, kim loại nóng chảy, muối nóng chảy, các mạng lưới liên kết cộng hóa trị nóng chảy, và các chất lỏng phân tử. Trong thực hành hóa học và hóa sinh, hầu hết các dung môi là chất lỏng phân tử. Chúng có thể được phân loại thành phân cực và không phân cực, tùy thuộc vào moment lưỡng cực điện của chúng. Một cách phân biệt khác là các phân tử của chúng có thể hình thành liên kết hiđrô hay không. Nước là dung môi thường được sử dụng nhất, là dung môi lưỡng cực và duy trì liên kết hydro.
Các muối hòa tan trong dung môi phân cực, tạo thành các ion dương và âm được thu hút đến gốc âm và dương của các phân tử dung môi tương ứng. Nếu dung môi là nước, sự hydrat hóa xảy ra khi các ion chất tan bị bao quanh bởi các phân tử nước. Một ví dụ tiêu chuẩn là nước muối. Những dung dịch như vậy được gọi là dung dịch điện giải.
Đối với các chất tan dạng không ion, thì có một quy luật chung: Giống nhau mới hòa tan vào nhau. Các chất tan phân cực hòa tan trong dung môi phân cực, tạo thành liên kết phân cực hoặc là liên kết hydro. Ví dụ, các thức uống có cồn đều là dung dịch dạng nước của ethanol. Trái lại, các chất tan không phân cực hòa tan tốt hơn trong dung môi không phân cực. Ví dụ, các hydrocacbon như dầu và mỡ dễ dàng trộn lẫn với nhau, nhưng không trộn với nước được.
Một ví dụ về sự không trộn lẫn với nhau của dầu và nước là những vết dầu loang trên mặt nước.
- Hoà vào nước ( không chắc lắm ạ ! )
Bột giấy :Hoà tan trong nước ( tuỳ từng loại )
Bột cát : Không hoà tan , chìm xuống đáy .