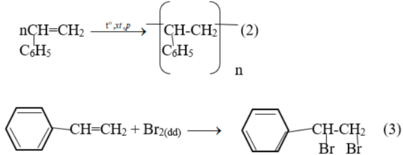
Cho 13 gam hỗn hợp gồm benzen và stiren làm mất màu vừa đủ dung dịch chứa 8 gam brom. Tỉ lệ mol benzen và stiren trong hỗn hợp ban đầu là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chỉ có stiren làm mất màu brom
\(C_8H_8+Br_2\rightarrow C_8H_8Br_2\)
0,2_______0,2_________
Đổi 100ml = 0,1l
\(n_{Br2}=0,1.2=0,2\left(mol\right)\)
\(m_{C8H8}=0,2.104=20,8\left(g\right)\)
\(m_{C6H6}=18,2-20,8=-2,6\left(?\right)\)

nBr2 = 0,06.0,15 = 0,009(mol)
Theo định luật bảo toàn khố lượng: mA = msriren = 52,00 (kg) = 52.103 (g)
Theo đề bài: 5,2 g A tác dụng vừa đủ với 0,009 mol Br2
52.103g A tác dụng vừa đủ với 90 mol Br2
Theo (3): nstiren = nBr2 = 90(mol)
mstiren = 90.104 = 9360(g) = 9,36(kg)
Khối lượng stiren đã tham gia trùng hợp = mA - mstiren = 52 - 9,36 = 42,64 (kg)

Chọn đáp án D
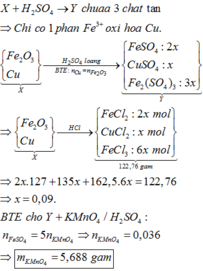
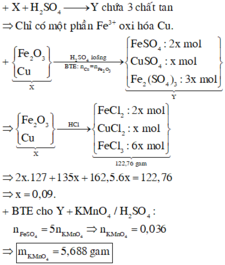
Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → n C u S O 4 : n F e S O 4 = 1 : 2 .
⇒ n C u S O 4 : n F e S O 4 : n F e 2 ( S O 4 ) 3 = 1 : 2 : 3 .
Đặt n C u S O 4 = x mol ⇒ n F e S O 4 = 2x mol và n F e 2 ( S O 4 ) 3 = 3x mol.
⇒ n C u 2 + = x mol; n F e 2 + = 2x mol; n F e 3 + = 6x mol
⇒ n C u C l 2 = x mol; n F e C l 2 = 2x mol; n F e C l 3 = 6x mol.
⇒ mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
⇒ Y chứa 0,18 mol FeSO4. Bảo toàn electron: 5 n K M n O 4 = n F e S O 4 .
![]()
![]()

Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
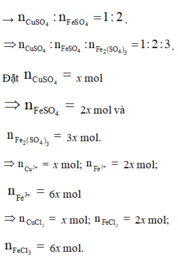
mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
Y chứa 0,18 mol FeSO4. Bảo toàn electron:
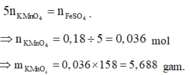
Đáp án D



\(Br2+C6H5CHCH2-->C6H5-CH\left(Br\right)-CH2Br\)
\(n_{Br2}=\frac{8}{160}=0,05\left(mol\right)\)
\(n_{stiren}=n_{Br2}=0,05\left(mol\right)\)
\(m_{stiren}=0,05.104=5,2\left(g\right)\)
\(m_{benzen}=13-5,2=7,8\left(g\right)\)
\(n_{benzen}=\frac{7,8}{78}=0,1\left(mol\right)\)
\(n_{benzen}:n_{stizen}=0,1:0,05=2:1\)
\(C_6H_5CHCH_2+Br_2\rightarrow C_6H_5CH\left(Br\right)-CH_2Br\)
Gọi benzen là a (mol) , stiren là b (mol)
\(78a+104b=13\)
\(\Rightarrow b=0,05\)
\(\Rightarrow a:b=0,1:0,05=2:1\)