Nung 32,67g KClO3 có 25% tạp chất(có xúc tác MnO2).Tính thể tích O2(đktc) thoát ra
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol của kali clorat
nKClO3 = \(\dfrac{m_{KClO3}}{M_{KClO3}}=\dfrac{29,4}{122,5}=0,24\left(mol\right)\)
a) Pt : 2KClO3 → 2KCl + 3O2\(|\)
2 2 3
0,24 0,36
Các chất trong phương trình :
KClO3 : kali clorat
KCl : kali clorua
O2 : khí oxi
b) Số mol của khí oxi
nO2 = \(\dfrac{0,24.3}{2}=0,36\left(mol\right)\)
Thể tích của khí oxi sinh ra
VO2 = nO2 . 22,4
= 0,36 . 22,4
= 8,064 (l)
c) Số mol của photpho
nP = \(\dfrac{m_P}{M_P}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Pt : 4P + 5O2 → 2P2O5\(|\)
4 5 2
0,2 0,36 0,1
Lập tỉ so sánh : \(\dfrac{0,2}{4}< \dfrac{0,36}{5}\)
⇒ Photpho phản ứng hết , Oxi dư
⇒ Tính toán dựa vào số mol Photpho
Số mol dư của oxi
ndư = nban đầu - nmol
= 0,36 - \(\left(\dfrac{0,2.5}{4}\right)\)
= 0,11 (mol)
Khối lượng dư của khí oxi
mdư = ndư . MO2
= 0,11 . 32
= 3,52 (g)
Số mol của đi photpho pentaoxit
nP2O5 = \(\dfrac{0,2.2}{4}=0,1\left(mol\right)\)
Khối lượng của đi photpho pentaoxit
mP2O5 = nP2O5 . MP2O5
= 0,1 . 142
= 14,2 (g)
Chúc bạn học tốt
Mình xin lỗi bạn nhé , mình không biết viết chất xúc tác : MNO2 lên chỗ phương trình , bạn tự bổ sung giúp mình nhé

\(n_{KClO_3}=\dfrac{29.4}{122.5}=0.24\left(mol\right)\)
\(2KClO_3\underrightarrow{^{^{t^0}}}2KCl+3O_2\)
\(0.24.....................0.36\)
KClO3 : Kali clorat
KCl : Kali clorua
\(V_{O_2}=0.36\cdot22.4=8.064\left(l\right)\)
\(b.\)
\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(4P+5O_2\underrightarrow{^{^{t^0}}}2P_2O_5\)
Lập tỉ lệ :
\(\dfrac{0.2}{4}< \dfrac{0.36}{5}\) => O2 dư
\(n_{O_2\left(dư\right)}=0.36-0.2\cdot\dfrac{5}{4}=0.11\left(mol\right)\)
\(m_{O_2}=0.11\cdot32=3.52\left(g\right)\)
\(m_{P_2O_5}=0.1\cdot142=14.2\left(g\right)\)
Chúc em học tốt nhé !

\(m_{KClO_3}=32,67.\dfrac{100-25}{100}=24,5025\left(g\right)\)
=> \(n_{KClO_3}=\dfrac{24,5025}{122,5}=0,20\left(mol\right)\)
PTHH: \(2KClO_3-t^o->2KCl+3O_2\)
Theo PT ta có: \(n_{O_2}=\dfrac{0,20.3}{2}=0,3\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)
Theo PT ta có: \(n_{KCl}=n_{KClO_3}=0,20\left(mol\right)\)
=> \(m_{KCl}=0,20.74,5=14,9\left(g\right)\)

a) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$n_{O_2} = \dfrac{3}{4}n_{Al} = 0,15(mol)$
$V_{O_2} = 0,15.22,4 = 3,36(lít)$
b) $2KClO_3 \xrightarrow{t^o,MnO_2} 2KCl + 3O_2$
$n_{KClO_3\ pư} = \dfrac{2}{3}n_{O_2} = 0,1(mol)$
$m_{KClO_3\ pư} = 0,1.122,5 = 12,25(gam)$
$\Rightarrow m_{KClO_3\ đã\ dùng} = 12,25 : (100\% - 10\%) = 13,61(gam)$

câu 5
nKMnO4=\(\dfrac{31,6.98\%}{158}\)=0,196(mol)
2KMnO4−to→K2MnO4+MnO2+O2
nO2(lt)=\(\dfrac{1}{2}\)nKMnO4=0,098(mol)
Vìhaohụt5%
⇒VO2(tt)=0,098.95%.22,4=2,08544(l)

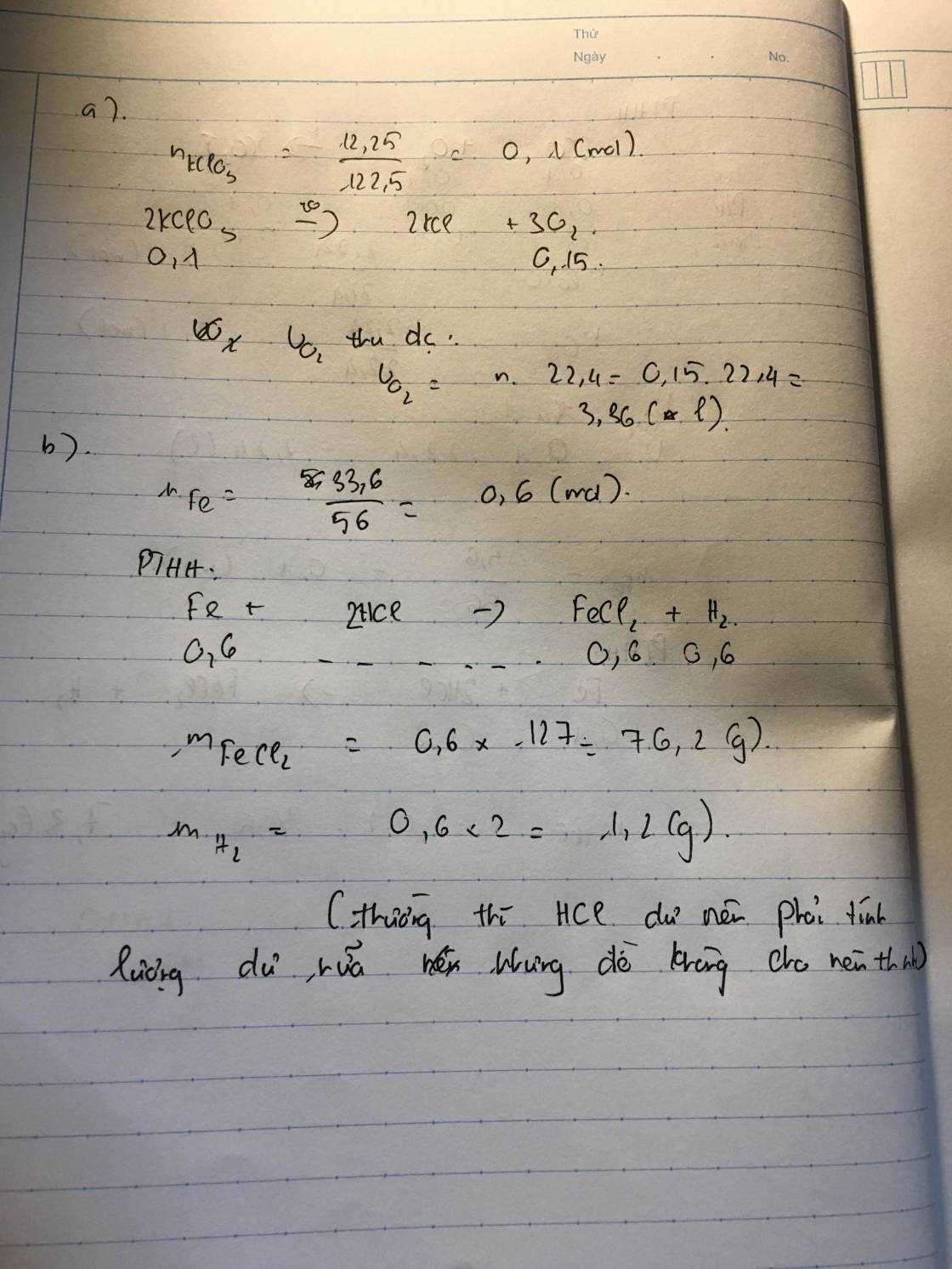
\(m_{KClO_3}=\left(100\%-25\%\right).32,67=24,5025\left(g\right)\)
=> \(n_{KClO_3}=\dfrac{24,5025}{122,5}=0,20\left(mol\right)\)
PTHH: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\)
Theo PT ta có: \(n_{O_2}=\dfrac{0,20.3}{2}=0,3\left(mol\right)\)
=> \(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
mKClO3 = 32,67.(100% - 25%) = 24,5025 (g)
nKClO3 = \(\dfrac{24,5025}{122,5}\) \(\approx\) 0,2 (mol)
2KClO3 \(\xrightarrow[MnO_2]{t^o}\)2KCl +3O2
Theo PT: nO2 = \(\dfrac{3}{2}\)nKClO3 = \(\dfrac{3}{2}.0,2\) = 0,3 (mol)
=> VO2 = 0,3.22,4 = 6,81 (l)
Vậy thể tích oxi thoát ra là 6,81 lít