đốt cháy 1,6 gam lưu huỳnh rồi cho sản phẩm cháy hấp thụ hoàn toàn vào 200ml dung dịch Ba(OH)2 0,5M .khối lượng kết tủa thu được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án D
Các chất trong X đều có CTPT là C4H8O2 và M = 88. nX = 0,075 mol.
Sơ đồ đốt: C4H8O2 → 4CO2 + 4H2O.
n C O 2 = n H 2 O = 4 n X = 0 , 3 m o l
m = 0,3.197 = 59,1 gam.
∆m = mdd sau = mdd trước = m2 - m1 = m C O 2 + m H 2 O – m
= 0,3.(44 + 18) – 59,1
= –40,5

Chọn đáp án D
n C O 2 = n C a C O 3 = 0 , 1 m o l
m d u n g d ị c h g i ả m = m C a C O 3 – ∑ ( m C O 2 + m H 2 O )
⇒ m H 2 O = 10 – 3 , 98 – 0 , 1 × 44 = 1 , 62 g a m
⇒ n H 2 O = 0 , 09 m o l .
X gồm C2H4O2, C3H4O, C4H6O2
⇒ nO = nH – nC = 0,09 × 2 – 0,1
= 0,08 mol.
⇒ mX = mC + mH + mO
= 0,1 × 12 + 0,09 × 2 + 0,08 × 16
= 2,66 gam.

Đáp án D
- Vì dùng 1 lượng dư Ca(OH)2 nên
![]()
![]()
![]()
- Xét hỗn hợp các chất lượng trọng X: HCOOCH3 (k=1); CH2=CH-CHO (k=2) và CH2=CH-COOCH3 (k=2)
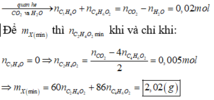
- Lưu ý: Nếu ta cho
![]()
thì lúc này ta sẽ giải ra được chính xác đáp án của đề bài cho.
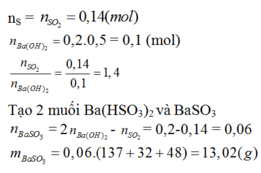

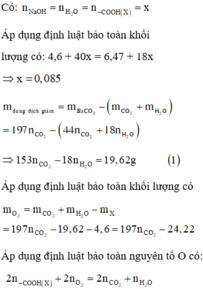
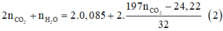
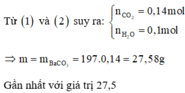
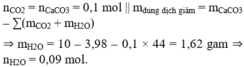
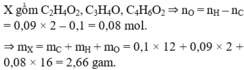
nS = 1,6/32 = 0,05
S + O2 → SO2
0,05 → 0,05
nOH- = 2nBa(OH)2 = 2.0,2.0,5 = 0,2
phương pháp : với bài toán cho SO2 tác dụng với kiềm thì
TH1 : nSO32- = nSO2 (nếu kiềm dư)
TH2 : nSO32- = nOH- - nSO2 (cả 2 chất cùng hết )
lưu ý: nSO32- <= nSO2
thường thì sẽ thử ở trường hợp 2 trước nếu nSO32- tính được ở TH2 <= nSO2 thì đó chính là nSO32- cần tìm. Nếu > nSO2 thì tính nSO32- theo TH1
ở TH2 : nSO32- = 0,2 - 0,05 =0,15 > 0,05 (loại)
⇒ tính theo TH1
nSO32- = nSO2 = 0,05
nBa2+ = nBa(OH)2 = 0,1 > nSO32- ⇒ nBaSO3 = nSO32- = 0,05
⇒m↓ = mBaCO3 = 0,05.197 = 9,85 g