Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl}=0,1.1=0,1\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,1.1=0,1\left(mol\right)\)
PTHH :
\(2HCl+Ba\left(OH\right)_2\rightarrow BaCl_2+2H_2O\)
trc p/u : 0,1 0,1
p/u : 0,1 0,05 0,05 0,1
sau p/u : 0 0,05 0,05 0,1
\(C_{M_{BaCl_2}}=\dfrac{0,05}{0,2}=0,25\left(M\right)\)
\(C_{M_{Ba\left(OH\right)_2dư}}=\dfrac{0,05}{0,2}=0,25\left(M\right)\)
\(m_{BaCl_2}=0,05.208=10,4\left(g\right)\)

Đáp án C.
n H C l = n A l a n = 0 , 12 m o l ; n N a O H ( d ư ) = 0 , 3 - 0 , 12 . 2 = 0 , 06 m o l
m r ắ n = m A l a n - N a + m N a C l + m N a O H d ư = 0 , 12 . 111 + 0 , 12 . 58 , 5 + 0 , 06 . 40 = 22 , 74 g a m

Đáp án D
H 2 NC 3 H 5 COOH 2 : 0 , 09 mol HCl : 0 , 2 mol + NaOH → H 2 NC 3 H 5 COONa 2 NaCl NaOH dư + H 2 O


Đáp án C
Có dung dịch X gồm NaCl (0,12 mol), và (NH4)2SO4 (0,025 mol)
(NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3 + 2H2O
Sau phản ứng dư: 0,005 mol Ba(OH)2 trong dung dịch
m= 0,12.58,5 + 0,005.171 = 7,875 gam

Đáp án:A
pH= 13 => [H+]=10-13M => [OH-]=10-1=0,1 M=> nOH-= 0,1.0,5=0,05 mol
mrắn = mKim loại + mOH- = 2,4 + 0,05.17= 3,25 gam

Đáp án B
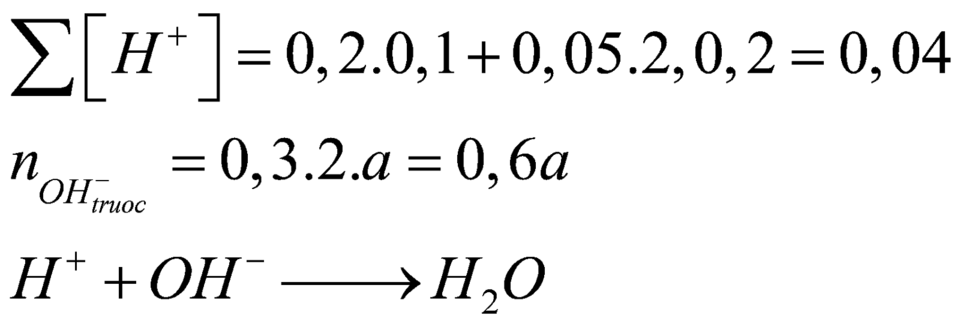
Mà sau phản ứng thu được dung dịch bazo có ph=13 (500ml)nên ta có
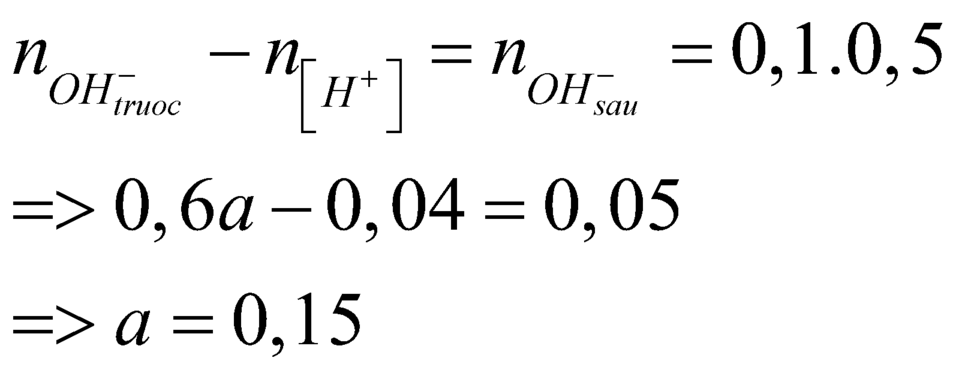
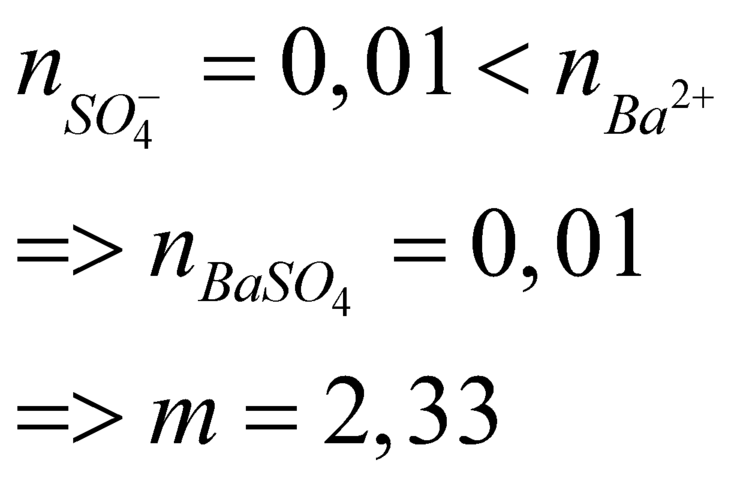
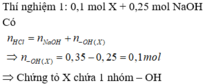

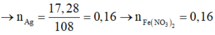
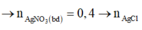
→ 0,015.35,5 + 0,2a.137 + 17(0,4a - 0,015) = 1,9875
→ a = 0,05 M
Đáp án D