Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Ta có: \(\dfrac{M_R}{M_R+32}\cdot100=46,67\) \(\Rightarrow M_R=28\)
Vậy R là Silic
b) Ta có: \(\dfrac{M_R}{M_R+4}\cdot100=87,5\) \(\Rightarrow M_R=28\)
Vậy R là Silic

Gọi công thức oxit sắt cần tìm là F e X O Y
Theo bài ta có: : = 7 : 3
Ta coi m F e = 7 gam; m O = 3 gam.
Khi đó:
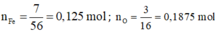
⇒ m C a O H 2 = 2.(40+17.2) = 148kg
⇒ n F e : n O = x : y = 0,125 : 0,1875 = 2 : 3
Vậy oxit sắt cần tìm là F e 2 O 3
⇒ Chọn A.

Câu 1: Chất tác dụng với nước tạo ra dung dịch bazơ là
A. CO2.
B. Na2O.
C. SO2.
D. P2O5.
Câu 2: Chất tác dụng với nước tạo ra dung dịch axit là
A. K2O.
B. CuO.
C. P2O5.
D. CaO.
Câu 3: Công thức hoá học của sắt (III) oxit là:
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Fe3O2.
Câu 4: 0,05 mol FeO tác dụng vừa đủ với:
A. 0,02 mol HCl.
B. 0,1 mol HCl.
C. 0,05 mol HCl.
D. 0,01 mol HCl.
Câu 5: Dãy chất nào sau đây là oxit lưỡng tính?
A. Al2O3, ZnO, PbO, Cr2O3.
B. Al2O3, MgO, PbO, SnO2.
C. CaO, ZnO, Na2O, Cr2O3.
D. PbO2, Al2O3, K2O, SnO2.
Câu 6: Hai oxit tác dụng với nhau tạo thành muối là:
A. CO2 và BaO.
B. K2O và NO.
C. Fe2O3 và SO3.
D. MgO và CO.
Câu 7: Một oxit của photpho có thành phần phần trăm của P bằng 43,66%. Biết phân tử khối của oxit bằng 142 đvC. Công thức hoá học của oxit là:
A. P2O3.
B. P2O5.
C. PO2.
D. P2O4.
Câu 8: Khí CO bị lẫn tạp chất là khí CO2. Cách làm nào sau đây có thể thu được CO tinh khiết?
A. Dẫn hỗn hợp qua dung dịch Ca(OH)2 dư.
B. Dẫn hỗn hợp qua dung dịch PbCl2 dư
C. Dẫn hỗn hợp qua NH3.
D. Dẫn hỗn hợp qua dung dịch Cu(NO3)2.
Câu 9: Cho 7,2 gam một loại oxit sắt tác dụng hoàn toàn với khí hiđro cho 5,6 gam sắt. Công thức oxit sắt là:
A. FeO.
B. Fe2O3.
C. Fe3O4.
D. FeO2.
Câu 10: Hoà tan 2,4 g một oxit kim loại hoá trị II cần dùng 30g dung HCl 7,3%. Công thức của oxit kim loại là:
A. CaO.
B. CuO.
C. FeO.
D. ZnO.

$n_{H_2SO_4} = 0,18(mol) \Rightarrow n_{H^+} = 0,18.2 = 0,36(mol)$
$n_{H_2} = \dfrac{0,336}{22,4} = 0,015(mol)$
$2H^+ + O^{2-} \to H_2O$
$2H^+ + 2e \to H_2$
Ta có :
$n_{H^+} = 2n_O + 2n_{H_2} \Rightarrow n_O = \dfrac{0,36 - 0,015.2}{2} = 0,165(mol)$
$\Rightarrow m = m_X - m_O = 11,04 - 0,165.16 = 8,4(gam)$



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


Hỗn hợp gồm Fe,Fe2O3,Fe3O4,FeO (coi hỗn hợp gồm Fe và O )
nFe=0,01 mol
=>nH2SO4 p/ư với Fe =0,01mol
=>nH2SO4 p/ư với oxit=0,11mol
=>n[O]=0,11mol
=> mFe ban đầu =7,36-0,01x16=5,6 g
Khi cho hh Fe,FeO,Fe3O4 vao dd H2SO4 thì thoát ra 0.01 mol H2 nên nFe trong hh =0.01mol
bạn để ý thấy trong oxits sắt thì có bao nhiêu ngtu O thì sẽ có bấy nhiêu gốc SO4 2- kết hợp vs Fe khi cho õit đó vào dd H2SO4 loãng
như vẬY nH2SO4 dùng để hoà tan oxits sắt là 0.12-nH2SO4(hoà tan Fe)=0.12-0.01=0.11
như vậy nO trong ôxuts sắt =nH2SO4 hoà tan ôxits sắt=0.11
nên m=7.36-0,11.16=5.6g

-Gọi công thức FexOy
%Fe=100%-22,22%=77,78%
\(x:y=\dfrac{77,78}{56}:\dfrac{22,22}{16}\approx1,4:1,4=1:1\)
Vậy oxit FeO đáp án B
B. FeO