Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khí O 2 khí này làm than hồng bùng cháy.
2KMn O 4 → K 2 Mn O 4 + O 2 + Mn O 2

Khí H 2 cháy trong không khí kèm theo tiếng nổ nhỏ.
H 2 SO 4 + Zn → Zn SO 4 + H 2
H 2 + 1/2 O 2 → H 2 O

Khí SO 2 khí này làm mất màu dung dịch KMn O 4
2 H 2 SO 4 + Cu → CuS O 4 + SO 2 + 2 H 2
2 H 2 O + 2KMn O 4 + 5 SO 2 → 2 H 2 SO 4 + 2MnS O 4 + K 2 SO 4
(không màu) (tím) (không màu, mùi sốc) (không màu) (trắng)

Khí Cl 2 khí clo ẩm có tính tẩy màu.
4HCl + MnO 2 → Mn Cl 2 + Cl 2 + 2 H 2 O

Thể tích khí hiđro :
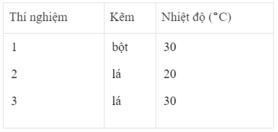
Sau các thí nghiệm, kẽm còn dư. Như vậy, thể tích khí hiđro được sinh ra phụ thuộc vào lượng H 2 SO 4 tham gia phản ứng
n H 2 = n H 2 SO 4 = 2.50/1000 = 0,1 mol
Thể tích khí hiđro ở điều kiện phòng là :
V H 2 = 0,1 x 24 = 2,4l = 2400 cm 3
Ta ghi số 2400 cm 3 trên trục y, nơi giao điểm giữa trục y và đường ngang của 3 đường cong kéo dài (nét chấm trên đồ thị).

Nhận xét:
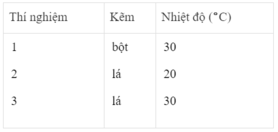
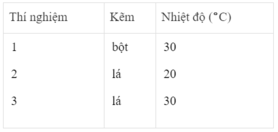
- Khí hiđro được giải phóng ở thí nghiệm 1 nhiều, nhanh hơn ở thí nghiệm 3. Vì diện tích tiếp xúc của Zn với H 2 SO 4 ở thí nghiệm 1 lớn hơn. trong khi đó nhiệt độ của dung dịch axit là như nhau.
- Khí hiđro được giải phóng ở thí nghiệm 3 nhiều, nhanh hơn ở thí nghiệm 2. Vì nhiệt độ của dung dịch H 2 SO 4 ở thí nghiệm 3 cao hơn, trong khi đó diện tích tiếp xúc giữa Zn và axit là như nhau.

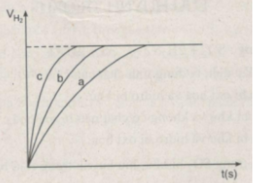
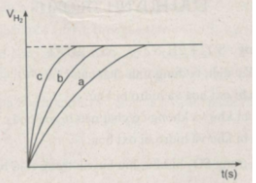
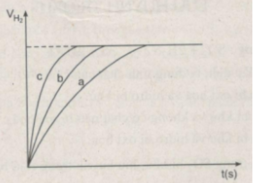
Đồ thị biểu diễn các phản ứng :
Đường cong c biểu diễn cho thí nghiệm 1, phản ứng xảy ra nhanh nhất
Đường cong b biểu diễn cho thí nghiệm 3, phản ứng xảy ra nhanh trung bình.
Đường cong a biểu diễn cho thí nghiệm 2, phản ứng xảy ra chậm nhất.

\(4H\mathop {Cl}\limits^{ - 1} {\text{ }} + {\text{ }}\mathop {Mn}\limits^{ + 4} {O_2} \to {\mathop {Cl}\limits^0 _2} + {\text{ }}\mathop {Mn}\limits^{ + 2} C{l_2} + {\text{ }}2{H_2}O\)
a)
\(\mathop {Mn}\limits^{ + 4} + 2e \to \mathop {Mn}\limits^{ + 2} \) => MnO2 là chất oxi hóa
\(\mathop {2Cl}\limits^{ - 1} \to \mathop {C{l_2}}\limits^0 + 2e\) => HCl là chất khử
b) HI có tính khử mạnh hơn HCl
=> HI có thể phản ứng được với MnO2
4HI + MnO2 → I2 + MnI2 + 2H2O

Cách 1: Cho hỗn hợp khí đi qua dung dịch HBr hoặc dung dịch HI, Cl 2 sẽ oxi hoá HBr hoặc HI thành Br 2 hoặc I 2 làm cho dung dịch không màu ban đầu chuyển thành màu vàng hoặc màu nâu.
Cl 2 + 2HBr → 2HCl + Br 2 (dung dịch có màu vàng)
hoặc Cl 2 + 2HI → 2HCl + I 2 (dung dịch có màu vàng nâu)
Cách 2: Có thể nhận ra Cl 2 có trong hỗn hợp khí bằng quỳ tím ấm.
Khi cho quỳ tím ẩm vào bình khí nếu quỳ tím ẩm chuyển sang màu đỏ sau đó mất màu đỏ chứng tỏ trong hỗn hợp khí có Cl 2


Khí CO 2 khẳng định bằng dung dịch Ca OH 2
CaCO 3 → CaO + CO 2
Ca OH 2 + CO 2 → CaCO 3 + H 2 O