Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Phương pháp điều chế clo trong phòng thí nghiệm: Đun nóng nhẹ dung dịch HCl đậm đặc với chất oxi hóa mạnh như MnO2 (hoặc KMnO4).
MnO2 + 4HCl \(\underrightarrow{t^o}\) MnCl2 + Cl2 + 2H2O
Để thu được khí clo tinh khiết:
- Bình H2SO4 đặc có tác dụng làm khô khí clo.
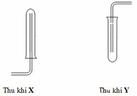
- Clo nặng hơn không khí Þ Thu bằng cách đẩy không khí.
- Bông tẩm xút: tránh để clo độc bay ra ngoài.

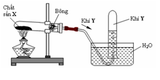
X là : dd HCl
Y là : Mn O 2 , KMn O 4
Phương trình hoá học của phản ứng điều chế clo.
Mn O 2 + 4HCl → Mn Cl 2 + 2 H 2 O + Cl2
2KMn O 4 + 16HCl → 2KCl + 2Mn Cl 2 + 5 Cl 2 + 8 H 2 O

4HCl + Mn O 2 → Mn Cl 2 + Cl 2 + 2 H 2 O
16HCl + 2KMn O 4 → 2KCl + 2Mn Cl 2 + 5 Cl 2 + 8 H 2
2NaCl + 2 H 2 O → 2NaOH + H 2 + Cl 2

- Dẫn hỗn hợp khí CO và CO 2 đi qua dung dịch NaOH hoặc Ca OH 2 . Khí ra khỏi dung dịch kiềm là khí CO vì khí CO 2 đã tác dụng với dung dịch NaOH hoặc Ca OH 2
CO 2 + 2NaOH → Na 2 CO 3 + H 2 O
CO 2 + Ca OH 2 → CaCO 3 + H 2 O
- Hoặc dẫn hỗn hợp khí qua canxi oxit (CaO), khí đi ra là khí CO.

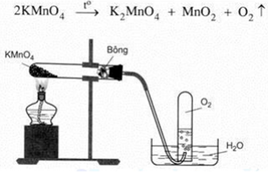
– Dùng phương pháp đẩy nước là hợp lí vì oxi ít tan trong nước và oxi thu được có độ tinh khiết cao.
– Oxi nặng hơn không khí, khi đốt nóng KMnO4 thì áp suất tại đó cao hơn nên
– Oxi sinh ra sẽ di chuyển xuống phía dưới ống nơi áp suất thấp hơn và dễ dàng thoát ra ống dẫn khí. – Bông khô có vai trò hút ẩm.
– Khi dừng thí nghiệm nên tắt đèn cồn trước sau đó mới tháo ống dẫn khí.

Đem nhiệt phân hỗn hợp muối thu được CO2, MgO, CaO
MgCO3 -> (t°) MgO + CO2
CaCO3 -> (t°) CaO + CO2
Thả hỗn hợp vào nước và thổi CO2 vào MgO không tan, CaO tan ta lọc lấy MgO
CaO + H2O -> Ca(OH)2
Ca(OH)2 + CO2 -> CaCO3 + H2O
CaCO3 + H2O + CO2 -> Ca(HCO3)2
Ta đem dd còn lại đi cô cạn ta được CaCO3
Ca(HCO3)2 -> (t°) CaCO3 + H2O + CO2
Đem CaCO3 đi nhiệt phân ta thu được CaO:
CaCO3 -> (t°) CaO + CO2
Đem CaO và MgO tác dụng lần lượt với dd HCl dư rồi lọc lấy MgCl2 và CaCl2 riêng biệt:
CaO + HCl -> CaCl2 + H2O
MgO + HCl -> MgCl2 + H2O

Chọn X: H2 ; Y : O2 ; Z: C2H2
Zn + 2HCl → ZnCl2 + H2
2KMnO4 →K2MnO4 + MnO2 + O2
CaC2 + 2H2O → Ca(OH)2 + C2H2

a. Khí O2 ít tan trong nước và nặng hơn không khí nên cách 1b không được (khi đó không khí sẽ xua hết khí O2 ra ngoài), trong phòng thí nghiệm người ta sử dụng cách 1a
b. Điều chế khí O2 người ta nhiệt phân các hợp chất giàu oxi: KMnO4; KClO3
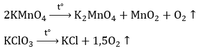

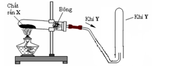
Phương pháp điều chế Clo trong phòng thí nghiệm
4HCl(dd đặc) +MnO2 -----------> MnCl2+ Cl2↑ +2H2O