Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 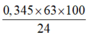
= 90,5625 gam

Đáp án A
Vì thể tích H2 sinh ra khi cho X tác dụng với H2O < thể tích khí H2 sinh ra khi cho X tác dụng với KOH dư.
⇒ Khi X tác dụng với H2O Al vẫn còn dư.
Đặt số mol Al = a và nNa = b.
+ Pứ với H2O Al còn dư ⇒ nAl pứ = nNa = b.
⇒ Bảo toàn e: 3b + b = 0,2×2 = 0,4 (1).
+ Pứ với KOH dư ⇒ Tan hoàn toàn.
⇒ Bảo toàn e: 3a + b = 0,35×2 = 0,7 (2).
+ Giải hệ (1) và (2) ⇒ nAl = 0,2 và nNa = 0,1.
⇒ mX = 0,2×27 + 0,1×23 = 7,7 gam

Đáp án : A
Khí X gồm : 0,15 mol H2 ; 0,15 mol C2H2 ; 0,45 mol CH4
=> mX = mY = 11,4g
Bảo toàn khối lượng : mY = mhc trong Br2 + mZ
=> mZ = 7,56g ; nZ = 0,51 mol
=> MZ = 14,82 => dZ/H2 = 7,41

Y chứa H2 → Z không chứa NO3-. Lập sơ đồ phản ứng:
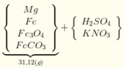
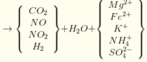
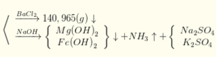
n(H2SO4) =n(SO42-) = n(BaSO4) = 0,605 mol; n(NH4+) = n(khí) = 0,025 mol
Áp dụng ĐLBT điện tích: n(Na+) + n(K+/Z) = 2n(SO42-)
→ n(KNO3) = n(K+) = 0,605*2 – 1,085 = 0,125 mol → (b) sai
Đặt n(Mg2+) = x; n(Fe2+) = y
→ (1) n(NaOH) = 2x + 2y + 0,025 = 1,085 mol
(2) m(kết tủa) = 58x + 90y = 42,9 gam
Giải (1) và (2): x = 0,15 mol; y = 0,38 mol → (e) đúng.
→ m = 0,15*24 + 0,38*56 + 0,125*39 + 0,025*18 + 0,605*96 = 88,285 gam → (a) sai
Áp dụng ĐLBT khối lượng: m(H2O) = 31,12 + 0,605*98 + 0,125*101 – 88,285 – 0,2*29,2 = 8,91
→ n(H2O) = 0,495 mol.
Áp dụng ĐLBT nguyên tố Hiđro: n(H2) = (0,605*2 – 0,025*4 – 0,495*2)/2 = 0,06 mol
Áp dụng ĐLBT nguyên tố Nitơ: Tổng n(NO, NO2) = tổng n(N/Y) = 0,125 – 0,025 = 0,1 mol
→ n(FeCO3) = n(CO2)= 0,2 – 0,1 – 0,06 = 0,04 mol; → %m(FeCO3) = 14,91% → (c) sai
m(X) = m(Mg) + m(Fe) + m(O) + m(CO32-) → m(O) = 31,12 – 0,15*24 -0,38*56 – 0,04*60 = 3,84
→ n(O) = 0,24 mol → n(Fe3O4) = 0,06 mol → (d) sai
Các kết luận không đúng là: (a); (b); (c); (d) → Đáp án D.

Chọn đáp án D
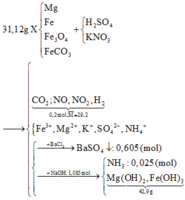
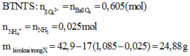
Quy đổi hỗn hợp X thành Fe, Mg, O và CO2
Đặt a, b là số mol của O và CO2 trong X. Đặt x là số mol H2
∑ m(O +CO2) = 31,12 – 24,88 = 6,24 (1)
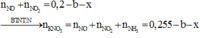
Sau phản ứng với dung dịch NaOH thu được dd chứa K2SO4 và Na2SO4
Bảo toàn điện tích:
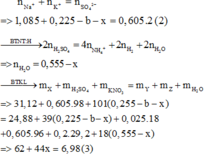
Từ (1), (2) và (3)
=> a = 0,28 (mol) ; b = 0,04 (mol) ; x = 0,06 (mol
=> m = 24,88 + 39 ( 0,255 –b –x) + 0,025.18 + 0,605.96 = 88, 285 => nhận định a) sai
nKNO3 = 0,225 – b – x = 0,125 => nhận định b) sai
%FeCO3 = ( 0,04.116/ 31,12).100% = 14,91% => nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => nhận định d) sai
=> có tất cả 4 nhận định sai.



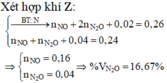


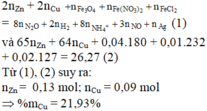
Đáp án : A
m gam X phản ứng với HCl tạo lượng khí lớn hơn khi phản ứng với H2O
=> Trong X có kim loại không phản ứng với H2O
Mà Y và Z thuộc 2 chu kỳ liên tiếp => Y là Mg(24) và Z là Ca(40)
Do nCa = nH2(1) = V 22 , 4 mol và nMg = nH2(2) – nCa = 2. V 22 , 4
=> Hỗn hợp kim loại có tỷ lệ mol Mg:Ca là 2:1
=> %mY(X) = 54,54%