
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



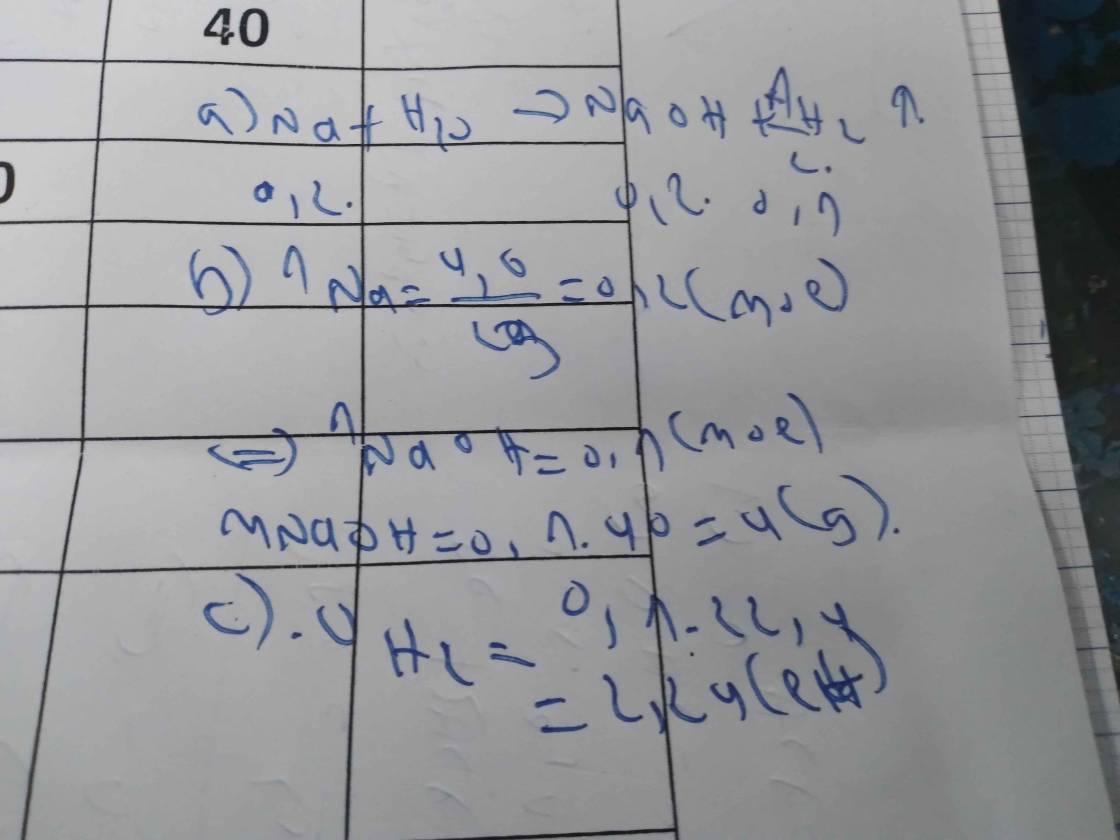
a) Pt: 2Na + 2H2O \(\rightarrow\) 2NaOH + H2
b) nNa = \(\dfrac{4,6}{23}=0,2mol\)
Theo pt: \(n_{H_2}=\dfrac{1}{2}n_{Na}=0,1mol\)
=> \(V_{H_2}=0,1.22,4=2,24l\)
c) Pt: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
nCuO = 16 : 80 = 0,2mol
Có nCuO : nH2 = \(\dfrac{0,2}{1}:\dfrac{0,1}{1}=2:1\)
=> CuO dư
Theo pt: nCu = nH2 = 0,1mol
=> mCu = 0,1.64 = 6,4g
a)
2Na + 2H2O ---> 2NaOH + H2.
b) Ta có:
nNa = 4,6/23 = 0,2 (mol)
Từ pt => nH2 = 0,2/2 = 0,1 (mol)
=> VH2 = 0,1.22,4 = 2,24 (lít)
c) CuO + H2 --to--> Cu + H2O
Ta có:
nCuO = 16/(64 + 16) = 0,2 (mol)
Lập tỉ lệ:
nCuO(tt)/nCuO(pt) = 0,2/1 = 0,2
nH2(tt)/nH2(pt) = 0,1/1 = 0,1
Vì 0,2 > 0,1 nên CuO dư
=> tính theo số mol của H2 => nCuO = 0,1 (mol)
Khối lượng chất rắn cần tìm là:
mCu = 0,1.64 = 6,4 (g)

\(n_{Zn}=\dfrac{26}{65}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.4.......0.8....................0.4\)
\(m_{HCl}=0.8\cdot36.5=29.2\left(g\right)\)
\(V_{H_2}=0.4\cdot22.4=8.96\left(l\right)\)

Số mol của 5,6g Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
a,\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b,thể tích của 0,1 mol H2:
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
c,\(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
khối lượng của 0,1 mol Cu:
\(m_{Cu}=n.M=0,1.64=6,4\left(g\right)\)

a)
\(Zn + 2HCl \to ZnCl_2 + H_2\)
b),c)
Theo PTHH :
\(n_{ZnCl_2} = n_{H_2} = n_{Zn} = \dfrac{13}{65} = 0,2(mol)\)
Vậy :
\(m_{ZnCl_2} = 0,2.136 = 27,2(gam)\\ V_{H_2} =0,2.22,4 = 4,48(lít)\)

a. Zn + 2HCl → ZnCl2 + H2
b. nZn = n\(_{ZnCl_2}\) =\(\dfrac{13}{65}=0,2\left(mol\right)\) => m\(_{ZnCl_2}\)= 0,2.136 = 27,2(g)
c. n\(_{H_2}\)= nZn = 0,2 (mol) => V\(_{H_2}\)=0,2.22,4 = 4,48 (lít)

\(n_{HCl}=0,2.2=0,4\left(mol\right)\\ a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.0,2........0,4.......0,2.......0,2\left(mol\right)\\ m=m_{Zn}=0,2.65=13\left(g\right)\\ c.m_{ZnCl_2}=136.0,2=27,2\left(g\right)\\ d.V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
Theo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
\(m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
c, \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{Cu}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)

a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Ta có: \(n_{Fe}=\dfrac{19,6}{56}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Fe}=0,35\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,35.22,4=7,84\left(l\right)\)
c, Ta có: \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{1}< \dfrac{0,35}{1}\), ta được H2 dư.
Theo PT: \(n_{H_2\left(pư\right)}=n_{CuO}=0,15\left(mol\right)\)
\(\Rightarrow n_{H_2\left(dư\right)}=0,35-0,15=0,2\left(mol\right)\)
\(\Rightarrow m_{H_2\left(dư\right)}=0,2.2=0,4\left(g\right)\)