Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
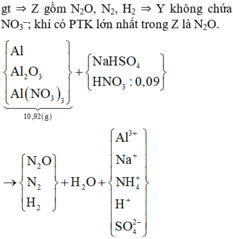
Ba 3 khí trong Z lần lượt là H2 (a mol), N2 (b mol) và N2O (c mol).
Dung dịch Y chứa NH4+ (x mol), Al3+ (y mol), H+ (z mol), SO42- (t mol), Na+ (t mol).
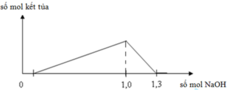
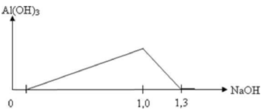
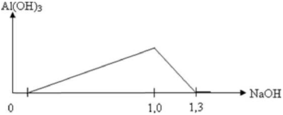
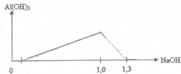
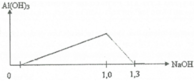
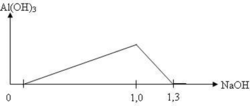
Tại n N a O H = 1 m o l ⇒ x + 3 y + z = 1 ( * ) n N a O H = 1 , 3 m o l ⇒ x + 4 y + z = 1 , 3 ⇒ y = 0 , 3 v à x + z = 0 , 1 ( 1 ) → B T D T ( Y ) x + z + 3 x + t = 2 t và x + z
Thay (*) vào suy ra: t = 1 mol
Mà mY =127,88 Þ 18x+z=0,78. Từ (1), (2) suy ra: x = 0,04 và y = 0,06
→ B T K L n H 2 O = 0 , 395 m o l sau đó tiếp tục → B T : H a = 0 , 04
Ta có: b + c = 0 , 04 28 b + 44 c = 1 , 52 ⇒ b = 0 , 015 c = 0 , 025 ⇒ % m N 2 O = 68 , 75 %

Đáp án B.
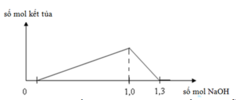
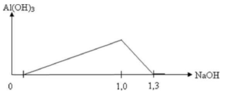
Xét đoạn 1,0 lên 1,3, ta suy ra được số mol Al3+ có trong dung dịch là 0,3 mol.
Y có chứa Al3+ (0,3 mol); Na+ (x mol), SO42- (x mol), NH4+ (y mol), H+ dự (z mol).
Kết tủa khi cực đại thì = 1 x = 1
Dựa vào hai phương trình BTĐT và BTKL muối 127,88 gam, ta có: y = 0,04; z = 0,06.
Ta có Z gồm ba khí H2, N2, N2O.
Bảo toàn khối lượng, ta tìm được
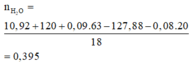
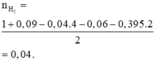
Từ đó suy được
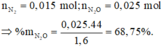

Đáp án B
Cho 5,52 gam Mg, Al tác dụng với 0,54 mol NaHSO4 và 0,08 mol HNO3 thu được dung dịch X chỉ chứa muối trng hòa và hỗn hợp Y gồm 3 khí không màu
Ta có: M - Y = 15 , 75
do vậy Y có H2, N2 và N2O
Cho NaOH dư vào X thu được kết tủa là Mg(OH)2
→ n M g = 0 , 14 → n A l = 0 , 08 m o l
Do dung dịch X chứa chứa muối trung hòa nên H+ hết, mặt khác do sinh ra khí H2 nên NO3- hết.
Dung dịch X sẽ chứa Mg2+ 0,14 mol, Al3+ 0,08 mol, NH4+, Na+ 0,54 mol và SO42-0,54 mol.
Bảo toàn điện tích: n N H 4 + = 0 , 02 m o l
Bảo toàn N: n N 2 + n N 2 O = 0 , 08 - 0 , 02 2 = 0 , 03 m o l
Gọi số mol N2, N2O và H2 lần lượt là a, b,c → a + b = 0 , 03 → 28 a + 44 b + 2 c a + b + c = 15 , 75
Bảo toàn e: 10a+8b+2c+0,02.8=0,14.2+0,08.3
Giải hệ: a=0,01; b=0,02; c=0,05
→ % H 2 = 7 , 94 %
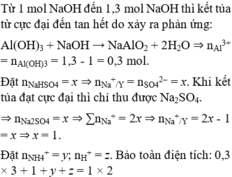


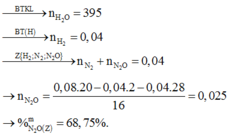


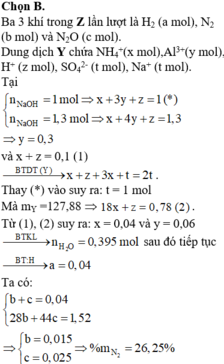


Chọn B