Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
\(Zn^0-2e\rightarrow Zn^{+2}|3\)
\(S^{+6}+6e\rightarrow S^0|1\)
Vậy ta có PTHH:
\(3Zn+4H_2SO_4--->3ZnSO_4+S+4H_2O\)
\(3Zn+4H_2SO_4->3ZnSO_4+S+4H_2O\)
Chất khử: Zn
Chất oxh: H2SO4
| Zn0-2e-->Zn+2 | x3 |
| S+6+6e --> S0 | x1 |

Đáp án A

Phương trình cân bằng:
( 5 x - 2 y ) F e 3 O 4 + ( 46 x - 18 y ) H N O 3 → ( 15 x - 16 y ) F e ( N O 3 ) 3 + N x O y + ( 23 x - 9 y ) H 2 O
=> Hệ số của HNO3 = (46x - 18y)

Mình nghĩ cái này thuộc kiến thức cơ bản, bạn nên tự học trong SGK thì hơn là đi đăng câu hỏi ở Hoc24

- Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
- Cân bằng hóa học là cân bằng động vì: Ở trạng thái cân bằng không phải là phản ứng dừng lại, mà phản ứng thuận nghịch và phản ứng nghịch vẫn xảy ra, nhưng tốc độ bằng nhau (Vthuận = Vnghịch). Điều này có nghĩa là trong một đơn vị thời gian số mol chất phản ứng giảm đi bao nhiêu theo phản ứng thuận lại được tạo ra bấy nhiêu theo phản ứng nghịch. Do đó cân bằng hóa học là cân bằng động.

- Hóa học nghiên cứu về thành phần, cấu trúc, tính chất và sự biến đổi của chất cũng như ứng dụng của chúng.
- Vai trò của hóa học trong đời sống và sản xuất
+ Là nhiên liệu dùng cho động cơ đốt trong
+ Làm vật liệu xây dựng
+ Ngành y tế: thuốc phòng, chữa bệnh cho người, chỉ khâu tự tiêu dùng trong y khoa
+ Làm mĩ phẩm, phân bón cho cây trồng
+ Nghiên cứu trong phòng thí nghiệm
- Phương pháp học tập và nghiên cứu hóa học một cách hiệu quả
+ Phương pháp học tập: (1) Phương pháp tìm hiểu lí thuyết, (2) Phương pháp học tập thông qua thực hành thí nghiệm, (3) Phương pháp luyện tập, ôn tập, (4) Phương pháp học tập trải nghiệm
+ Phương pháp nghiên cứu hóa học: (1) Xác định vấn đề nghiên cứu, (2) Nêu giả thuyết khoa học, (3) Thực hiện nghiên cứu (lí thuyết, thực nghiệm, ứng dụng), (4) Viết báo cáo: thảo luận kết quả và kết luận vấn đề

a) Cu + 2H2SO4 đặc->CuSO4+SO2+2H2O
b) Fe + H2SO4 đặc nguội-> ko pứ
c) 2H2SO4 đặc + S->3SO2+2H2O
d) H2SO4 đặc + KBr-> K2SO4 + Br2 + SO2 + 2H2O
e) H2SO4 đặc nguội + Al-> kopu
g) H2SO4 đặc + FeO->Fe2(SO4)3 + SO2 + H2O
h)4 H2SO4 đặc + 2Fe(OH)2->Fe2(SO4)3 + SO2 +6 H2O
i)6 H2SO4 đặc , dư + 2Fe (t0)->Fe2(SO4)3 +3 SO2 +6 H2O
m) C+ 2H2SO4 đặc-> CO2+2SO2+2H2O
n) H2SO4 đặc + 2NaOH->Na2SO4+2H2O
o) H2SO4 đặc + MgO->MgSO4+H2O
k)3 H2SO4 đặc + Fe2O3->Fe2(SO4)3+3H2O

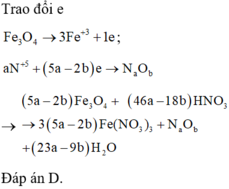

Cách viết phương trình hóa học là:
B1: Đọc kĩ đề bài
B2: Sắp xếp các chất tham gia mà đề cho vào vế trái và các chất tạo thành sản phẩm vào vế phải.
B3: Cân bằng vào phương trình
Cách để cân bằng phương trình hóa học là:
B1:Cân bằng kim loại trước tiên
B2: Cân bằng tới nhóm nguyên tử ( CO3;NO3;SO4;......)
B3:Cân bằng phi kim
B4: Cân bằng hiđro (H2)
B5: Cân bằng oxi (O2)
B6:Kiểm tra kết quả (bằng việc đếm số oxi ở hai vế phải bằng nhau)
Các công thức tính ở hóa học lớp 8:
\(.n=\frac{m}{M}\)
\(\Rightarrow m=n\times M\)
\(.n=\) (số nguyên tử/phân tử ): \(6\times10^{23}\)
\(.n=\frac{V_{Khí}}{22,4}\)
\(\Rightarrow V_{Khí}=n\times22,4\) (đktc)
\(.C_{Mdd}=\frac{n_{ct}}{V_{dd}}\)
\(\Rightarrow n_{ct}=C_{Mdd}\times V_{dd}\)
\(.V_{dd}=\frac{m_{dd}}{D_{dd}}\)
\(\Rightarrow m_{dd}=D_{dd}\times V_{dd}\)
\(.C\%=\frac{m_{ct}}{m_{dd}}\times100\%\)
\(.m_{dd}=D_{dd}\times V_{dd}\)
\(.m_{dd}=m_{ct}+m_{H_2O}\)
\(.m_{ddsau}=\) tổng m chất tham gia - m \(\downarrow\) (kết tủa) - m \(\uparrow\) (bay hơi)