Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
♦ YTHH 03: sinh 0,14 mol H2 ||→ thêm 0,14 mol O vào 40,1 gam hỗn hợp
chuyển về 42,34 gam chỉ gồm oxit Na2O và BaO; từ 0,28 mol NaOH → có 0,14 mol Na2O
||→ có 0,22 mol BaO → đọc ra 0,22 mol Ba(OH)2 ||→ X chứa 0,72 mol OH–.
Phản ứng: 2OH– + CO2 → CO32– + H2O || OH– + CO2 → HCO3–.
biết nCO2 = 0,46 mol ||→ sau phản ứng có: 0,26 mol CO22– và 0,2 mol HCO3–.
0,22 mol Ba2+ và 0,28 mol Na+ ||→ đọc ra Y gồm: 0,04 mol Na2CO3 và 0,2 mol NaHCO3.
Mặt khác, 200 ml dung dịch Z gồm (0,08 + y) mol H+ ||→ a = 2,5y là giá trị cần tìm.
► giải theo trắc nghiệm: chọn TH khó nhất để giải (tự luận sẽ phải chặt chẽ hơn, xét thêm TH).
♦ cho H+ từ từ vào Y: H+ + CO3– → HCO3– trước, sau đó: H+ + HCO3– → CO2↑ + H2O.
DỰa vào số liệu → nCO2 = (0,08 + y) – 0,04 = x (1).
♦ Cho ngược lại: xảy ra đồng thời: HCO3– + H+ → CO2 + H2O || CO32– + 2H+ → CO2 + H2O.
giả sử có z mol CO32– phản ứng thì tương ứng có 5z mol HCO3– phản ứng (tỉ lệ 0,04 ÷ 0,2 = 1 ÷ 5)
||→ ∑nkhí CO2 = z + 5z = 1,2x và ∑nH+ = 2z + 5z = 7z = 0,08 + y ||→ 1,4x = 7z = 0,08 + y (2).
Giải (1) và (2) ||→ x = 0,1 mol và y = 0,06 mol ||→ a = 2,5y = 0,15.

Đáp án A
· Có n FeCO 3 = n CO 2 = n CaCO 3 = 24 100 = 0 , 24 mol
· Phần 1: n Al = 2 3 n H 2 = 2 3 . 0 , 06 = 0 , 04 mol
Þ Al dư, hỗn hợp rắn sau phản ứng gồm Fe, Al2O3.
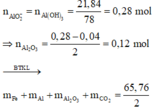 ⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
· Phần 2: Đặt số mol muối Fe2(SO4)3 và FeSO4 lần lượt là x, y.
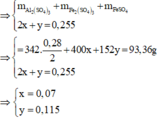
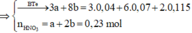
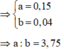

Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m B nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.

Đáp án B
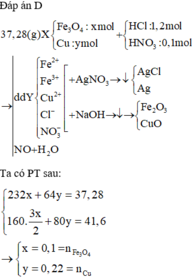
Đặt nFe₃O₄ = x; nCu = y ⇒ mX = 232x + 64y = 37,28(g).
~ Chú ý: "hòa tan hết" ⇒ toàn bộ nguyên tố Fe và Cu sẽ đi hết vào oxit :P
Mặt khác, nung trong KHÔNG KHÍ
⇒ oxit là Fe₂O₃ (1,5x mol) và CuO (y mol).
⇒ m oxit = 41,6(g) = 160.1,5x + 80y
⇒ giải hệ có: x = 0,1 mol; y = 0,22 mol
► nHCl = 1,2 mol; nHNO₃ = 0,1 mol
⇒ nH⁺ = 1,3 mol; nNO₃⁻ = 0,1 mol.
Do Y + AgNO₃ -> sinh ra khí NO
⇒ Y có chứa H⁺, Fe²⁺ và không chứa NO₃⁻
(vì nếu có NO₃⁻ sẽ phản ứng sinh ra NO rồi :P)
Bỏ qua phần H⁺ "trung hòa" oxi trong oxit: 2H⁺ + O → H₂O thì còn
nH⁺ = 1,3 - 0,4 × 2 = 0,5 mol
● Xét toàn bộ các quá trình cho - nhận electron:
– Cho e: 3Fe⁺⁸/₃ → 3Fe⁺³ + e
Cu → Cu²⁺ + 2e
– Nhận e: 4H⁺ + NO₃⁻ + 3e → NO + 2H₂O
Ag⁺ + e → Ag
Do NO₃⁻ cả quá trình dư (vì AgNO₃ dư) nên:
⇒ bảo toàn electron cả quá trình:
nFe₃O₄ + 2nCu = ³/₄nH⁺ + nAg
⇒ nAg = 0,165 mol (nH⁺ đây là nH⁺ không tính phần "trung hòa" oxi trong oxit )
BTNT(Cl) ⇒ nAgCl = nHCl = 1,2 mol
⇒ m = 0,165 × 108 + 1,2 × 143,5 = 190,02(g)

Đáp án C
Sau phản ứng thu được hỗn hợp kim loại C => Chứng tỏ C chứa Ag, Cu, có thể có Fe dư, Al dư.
Có khối lượng chất rắn thu được ở phần 1 nhiều hơn phần 2 => Chứng tỏ trong dung dịch ngoài Al(NO3)3 còn chứa Fe(NO3)2
=> Al, Cu(NO3)2 và AgNO3 phản ứng hết, Fe có thể còn dư.
Đặt số mol Cu(NO3)2 và AgNO3 lần lượt là a, b.
Đặt số mol Al và Fe phản ứng lần lượt là x, ỵ
Chất rắn thu được ở phần 2 là Fe2O3 => 160.0,5y = 6,2 => y = 0,15
Chất rắn thu được ở phần 1 là Al2O3 và Fe2O3
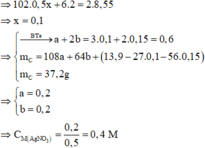

Đáp án C
NHận thấy nX : nNaOH =0,08 :0,08 = 1:1 → X có 1 nhóm COOH và số mol nước sinh ra là 0,08 mol
Bảo toàn khối lượng → m X = 10 +0,08. 18 - 0,08. 40 = 8,24 gam → MX = 8,24 : 0,08 = 103

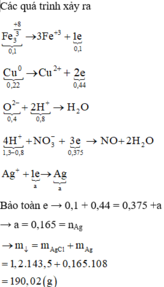


MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O (1)
0,8 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O (2)
0,1 0,2 mol 0,1
Cl2dư + H2O → HCl + HClO (3)
0,7 0,7
→ nCl- = 0,8 mol → [Cl-] = 0,8/0,5 = 1,6 M.
help me