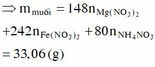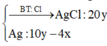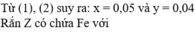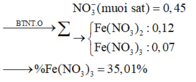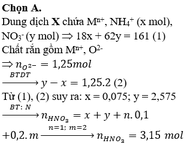Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

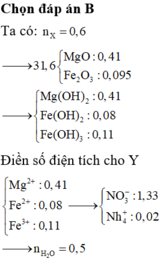
Chọn đáp án B
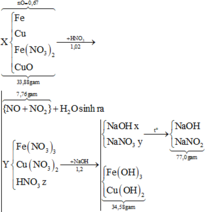
Ta có: 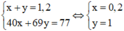
đặt z là nHNO3 dư, BTNT.H Þ nH2O sinh ra = 0,51 – 0,5z
BTNT.N Þ n N O 3 - trong muối của Y là 1 – z = nOH trong kết tủa
Þm Kim loại = 34,58 – 17x(1-z) gam
BTKL Þ 33,88 + 1,02x63 = 34,58 - 17x(l - z) + z + 62 + 7,76 + (0,51 - 0,5z)xl8 Þ z = 0,18

BTNT.N Þ nFe(NO3)2 = (0,09 + 0,11 + 1 -1,02)/2 = 0,09 Þ nFe = 0,14 - 0,09 = 0,05
Vậy %m Fe trong X ![]()

Đáp án D
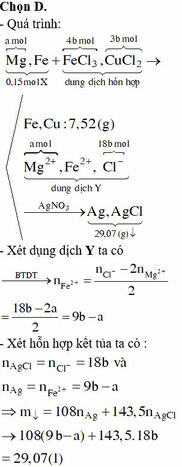
Ta có: n FeCl 3 = 0 , 16 ; n CuCl 2 = 0 , 12
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl 0,72 mol (bảo toàn nguyên tố Cl) và Ag 0,06 mol.
Nếu cho NaOH dư vào X thì lượng NaOH phản ứng 0,78 mol, do vậy
n Al = 0 , 78 - 0 , 72 = 0 , 06 mol
Do n Ag = 0 , 06 → n Fe + 2 trong X = 0 , 06 mol
Ta có: n Fe 2 + < n FeCl 3 và khối lượng rắn tăng do vậy Fe dư
Gọi số mol Mg là a mol, Fe là b mol
→ m = 24a+56b+0,06.27
Rắn Y sẽ chứa Cu 0,12 mol và Fe 0,1+b mol
→ 1,8275m = 0,12.64+56(0,1+b)
Dung dịch X chứa MgCl2 a mol, AlCl3 0,06 mol và FeCl2 0,06 mol
→ a = 0 , 72 - 0 , 06 . 3 - 0 , 06 . 2 2 = 0,21 mol → b = 67 2800
→ m = 8 gam

Đáp án B
Thêm AgNO3 vào Y ® NO chứng tỏ trong Y có chứa cặp H+ và Fe2+ ® anion trong Y chỉ có Cl- mà thôi.
Lượng H+ dư được tính nhanh = 4nNO = 0,18 mol ® lượng phản ứng là 1,64 mol. Sơ đồ:
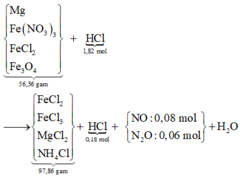
« Bảo toàn khối lượng cả sơ đồ có m H 2 O = 13 , 32 g a m → n H 2 O = 0 , 74 m o l
Theo đó, bảo toàn nguyên tố H có 0,04 mol NH4Cl và có 0,08 mol Fe(NO3)3 (theo bảo toàn N sau đó).
Tiếp tục theo bảo toàn electron mở rộng hoặc dùng bảo toàn O có ngay số mol Fe3O4 là 0,04 mol.
« Gọi số mol Mg và FeCl2 trong X lần lượt là x, ymol ® 24x + 127y = 27,72 gam.
Xét toàn bộ quá trình, bảo toàn electron ta có:
2 x + y + 0 , 04 = 8 × 0 , 04 + ( 0 , 08 + 0 , 045 ) × 3 + 0 , 06 × 8 + n A g → n A g = ( 24 x + Y - 1 , 1350 ) m o l
Lại có: . Tổng khối lượng kết tủa là 298,31 gam.
® có phương trình: 143,5.(2y+1,82)+108.(2x+y-1,135=298,31
Giải hệ các phương trình trên được x = 0,52 mol; y = 0,12 mol.
vậy yêu cầu: % m F e C l 2 t r o n g X = 0 , 12 × 127 56 , 36 × 100 % ≈ 27 , 04 % .

Đáp án B
Do dung dịch Y tăng 21,28 gam.
→ m X = 28 , 96 - 21 , 28 = 7 , 68 g a m T a c ó : n X = 7 , 68 9 , 6 . 4 = 0 , 2 m o l
Do vậy ta giải được số mol CO2 và NO trong X lần lượt là 0,06 mol và 0,08 mol.
Vậy số mol FeCO3 là 0,06 mol.
Do khi thêm AgNO3 vào Y có xuất hiện NO nên H+ dư nên Y không có NO3- dư.
Bảo toàn N: n N H 4 + = 0 , 24 - 0 , 06 . 2 - 0 , 08 = 0 , 04 m o l
Gọi a, b lần lượt là số mol Mg, Fe3O4, c là số mol HCl.
Do vậy kết tủa chứa AgCl c mol và Ag.
→ 24 a + 232 b + 0 , 06 . 116 = 28 , 96
Do cho AgNO3 vào sinh ra 0,03 mol NO nên H+ dư 0,12 mol.
Bảo toàn e kết hợp bảo toàn điện tích:
c= 0,04+8b+0,06.2+0,08.3+0,06.8+0,04.8+0,12
Bảo toàn e:
n A g = 2 a + b + 0 , 06 - 0 , 04 . 8 - 0 , 08 . 3 - 0 , 03 . 3 - 0 , 06 . 8 = 2 a + b - 1 , 07 → 143 , 5 c + 108 ( 2 a + b - 1 , 07 ) = 238 . 58
Giải được: a=0,53; b=0,04; c=1,64.
%Mg= 43,92%