Câu 1: Biểu thức tính pH của dung dịch theo nồng độ ion là
A. pH = log .
C. pH = log .
B. pH = - log .
D. pH = - log .
Câu 2: Phát biểu đúng về bazơ theo thuyết a-re-ni-ut là
A. Bazơ là những chất khi phân li trong dung dịch ra anion OH-.
B. Bazơ là những chất khi phản ứng cho anion OH-.
C. Bazơ là những chất khi phân li trong dung dịch ra cation H+.
D. Bazơ là những chất khi phản ứng cho cation H+.
Câu 3: Cho các dung dịch HNO3 0,001M(1), NaOH 0,01M(2), H2SO4 0,005M(3), pH có giá trị tăng dần theo thứ tự là
A. 1, 2, 3.
C. 3, 1, 2.
B. 1, 3, 2.
D. 3, 2, 1.
Trong phản ứng: N2 + 4H2SO4(đặc) ¾¾® 4SO2 + 2NO2 + 4H2O; N2 đóng vai trò là
A. Chất khử.
B. Chất oxi hoá.
C. Vừa là chất khử vừa là chất oxi hoá.
D. Axit.
Câu 6: Cho a gam P tác dụng với 100ml HNO3 1M, thu được V lít NO2 đktc. Giá trị của a và V lần lượt là
A. 0,62 gam; 1,12 lít.
C. 3,1 gam; 1,12 lít.
B. 0,62 gam; 2,24 lít.
D. 3,1 gam; 2,24 lít.
Câu 7: Chất nào sau đây không thuộc là dạng thù hình của cacbon?
A. Kim cương.
B. Than chì.
C. Kính.
D. Feleren.
Câu 8: Sođa khan có công thức phân tử là
A. Ca(HCO3)2.
B. NH4HCO3.
C. CaCO3.
D. Na2CO3.
Câu 9: Trong phòng thí nghiệm CO2 được điều chế bằng cách cho dung dịch HCl tác dụng với chất nào sau đây?
A. CO2.
B. CaCO3.
C. CO.
D. H2CO3.
Câu 10: C và CO khử được dãy oxit kim loại nào dưới đây?
A. NaO, CuO, ZnO.
C. HgO, CuO, BaO.
B. CuO, Al2O3, Fe2O3.
D. HgO, CuO, Fe2O3.
Câu 11: Tổng hệ số cân bằng trong phản ứng: C + H2SO4(đặc)¾¾® CO2 + SO2 + H2O bằng
A. 2.
C. 6.
B. 4.
D. 8.
Câu 12: Cho a gam C tác dụng với khí H2 thu được 4,48 lít CH4 điều kiện tiêu chuẩn. Giá trị của a là
A. 0,6 gam.
C. 1,8 gam.
B. 1,2 gam.
D. 2,4 gam.
Câu 18: Hợp chất hữu cơ A có công thức tử C2H6, liên kêt hoá học trong A là
A. Liên kết ion.
C. Liên kết kim loại.
B. Liên kết cộng hoá trị.
D. Liên kết cộng hoá trị cho nhận.
Câu 19: Để xác định nguyên tố N trong một số hợp chất hữu cơ đơn giản trong phương pháp phân tích định tính nguyên tố người ta chuyển nguyên tố N trong hợp chất hữu cơ thành chất nào sau đây?
A. HNO3.
C. NH3.
B. NH4NO3.
D. NO2.
Câu 20: Nhận xét nào sau đây không đúng khi nói về hợp chất hữu cơ A có công thức phân tử là C2H6?
A. Trong hợp chất hữu cơ A có 2 nguyên tử cacbon và 6 nguyên tử oxi.
B. Công thức đơn giản nhất của hợp chất hữu cơ A là CH3.
C. Hợp chất hữu cơ A có cùng công thức đơn giản với hợp chất hữu cơ B (C2H6O)
D. Công thức CH3 là tỉ lệ tối giản về số lượng nguyên tố trong hợp chất hữu cơ A.
Câu 21: Hợp chất hữu cơ X có công thức đơn giản nhất là CH3O. Biết số lượng nguyên tử của các nguyên tố trong công thức phân tử của X gấp 2 lần công thức đơn giản nhất. Công thức phân tử của X là
A. C2H6O2.
C. CH6O2.
B. C2H6O.
D. CH3O.
Câu 22: Axit axetic (CH3COOH) và đường glucozơ (C6H12O6) có cùng công thức đơn giản nhất là
A. C2H3O2.
B. C2HO.
C. CH2O.
D. CHO2.
Câu 23: Hợp chất hữu cơ A có tỉ khối so với khí oxi bằng 1,4375. Khối lượng mol phân tử của A bằng
A. 23 gam/mol.
B. 46 gam/mol.
C.41,6875gam/mol.
D. 40,25 gam/mol.
Câu 24: Phân tích nguyên tố trong hợp chất khí metan cho thấy C chiếm 75% về khối lượng, còn lại là H. Công thức đơn giản nhất của metan là
A. C6H25.
B. C6H4.
C. CH4.
D. C2H8.
Câu 25: Chất nào sau đây chứa liên kết đôi trong công thức cấu tạo?
A. C2H6.
B. C2H4.
C. C2H2.
D. C3H8.
Câu 26: Cho các hợp chất hữu cơ A, B có công thức phân tử lần lượt là C2H6O và C3H8O. A và B được gọi là
A. Đồng vị.
C. Đồng đẳng.
B. Đồng phân.
D. Đồng phân mạch cacbon.
Câu 27: Cho các hợp chât hữu cơ A, B có công thức câu stạo lần lượt là CH3 – CH2 – OH, CH3 – O – CH3. A và B được gọi là
A. Đồng vị.
C. Đồng đẳng.
B. Đồng phân.
D. Đồng phân mạch cacbon.
Câu 28: Hợp chất hữu cơ A có công thức phân tử là C3H6. Chất nào sau đây là đồng đẳng của A?
A. C4H8.
C. C3H8.
B. C4H10.
D. C2H6.



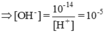


a)
pH = 2
=> [H+] = 10-2 M
=> \(\left[OH^-\right]=\dfrac{10^{-14}}{10^{-2}}=10^{-12}M\)
b)
pH = 10
=> \(\left[H^+\right]=10^{-10}M\)
=> \(\left[OH^-\right]=\dfrac{10^{-14}}{10^{-10}}=10^{-4}M\)
c) pH = 6
=> \(\left[H^+\right]=10^{-6}M\)
=> \(\left[OH^-\right]=\dfrac{10^{-14}}{10^{-6}}=10^{-8}M\)
d)
pH = 8
=> \(\left[H^+\right]=10^{-8}M\)
=> \(\left[OH^-\right]=\dfrac{10^{-14}}{10^{-8}}=10^{-6}M\)