Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2KClO3 -> 2KCl + 3O2
b) MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
b) SGK

b1: viết pthh
cl2+ h2-> 2hcl
b2: tính số mol cá chất dựa vào khối lượng hoăc thể tích đề bài cho
nH2= 67,2/224=3 mol
b3: dựa vào phương trình tính số mol các chất còn lại
theo pthh: ncl2=nh2=3 mol
nhcl=2nh2=3*2=6 mol
b4: tính khối lượng hoặc thể tích chất đề bài yêu cầu
=> Vcl2= 3*22,4=67,2l
mhcl=6* 36,5= 219g
CHÚC BẠN HỌC TỐT!

Có: nH2= 67,2:22,4=3(mol)
PTPƯ: H2 + Cl2 --to--> 2 HCl
(mol) 1 1 2
(mol) 3 3 6
(l) 67,2 67,2 134,4
(g) 6 213 219

Câu 2:
- Khác nhau:
+) P/ứ phân hủy: Từ 1 chất tạo ra nhiều chất
+) P/ứ hóa hợp: Từ nhiều chất tọa ra 1 chất
- VD: \(K_2O+CO_2\rightarrow K_2CO_3\) (P/ứ hóa hợp)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\) (P/ứ phân hủy)
Câu 3:
a) PTHH: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\uparrow\)
b) P/ứ trên thuộc p/ứ phân hủy vì từ 1 chất là CaCO3 tạo ra 2 chất mới (CaO và CO2)
Phòng thí nghiệm | Công nghiệp | |
Nguyên liệu | KMnO4, KClO3 | không khí, nước |
Sản lượng | đủ để làm thí nghiệm | sản lượng lớn |
Giá thành | cao | thấp |


1. Cách thu khí oxygen? Giải thích
Đẩy nước do khí Oxi ít tan trong nước hoặc thu bằng cách ngửa bình do khí Oxi nặng hơn không khí
2.cách thu khí hidrogen? Giải thích
Đẩy nước do khí hidrogen ít tan trong nước hoặc thu bằng cách úp bình do khí hidrogen nhẹ hơn không khí

1. Tính khối lượng chất tham gia và sản phẩm
* Các bước giải:
- Đổi số liệu đầu bài. Tính số mol của chất mà đầu bài cho.
- Lập phương trình hoá học.
- Dựa vào số mol chất đã biết để tính số mol chất cần tìm.
2. Tính thể tích khí tham gia và tạo thành
H2+Cl2->2HCl
\(n_{H_2}=67,2:22,4=3\left(mol\right)\)
Ta có: \(n_{H_2}=n_{Cl_2}=3\left(mol\right)\)
\(V_{Cl_2}=3.22,4=67,2l\)
\(n_{HCl}=2n_{Cl_2}=2.3=6\left(mol\right)\)
\(m_{HCl}=6.36,5=219g\)

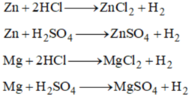
Điều chế khí oxi:Trong phòng thí nghiệm:\(2KClO_3->2KCl+3O_2\left(đktđ\right)\)
Điều chế khí oxi:Trong công nghiệp \(2H_2O->2H_2+O_2\left(đktđ\right)\)
Điều chế khí hiđro:Trong công nghiệp \(2H_2O->2H_2+O_2\left(đktđ\right)\)
Điều chế khí hidro:Trong phòng thí nghiệm:\(Fe+2HCl->FeCl_2+H_2\)
hoặc:\(Fe+H_2SO_4->FeSO_4+H_2\)
Chú thích:Đktđ:Điều kiện nhiệt đố
\(Fe+2HCl->FeCl_2+H_2\)
à tôi viết nhầm:Ở đây phải là điều kiện nhiệt độ mới đúng