hỗn hợp X gồm Nitơ và Hidro có tỉ khối so với Hidro là 3,6. Nung nong X với xúc tác thích hợp, lúc đó xảy ra phản ứng. H2 + N2 -> NH3. Sau phản ứng thu được hỗn hợp khí Y có tỉ khối so với Hidro là 4,2826. Tính hiệu suất tổng hợp NH3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đây là một ví dụ rất đơn giản nhưng đặc trưng về quan hệ số mol trong phản ứng cộng hidro của hidrocacbon chưa no
Dễ tính đươc
![]()
Trong phản ứng hidro hóa hidrocacbon chưa no thì số mol khí giảm chính bằng số mol hidro phản ứng suy ra ![]()
Mặt khác đề cho hidrocacbon dư, phản ứng hoàn toàn nên
![]()
suy ra ![]()

Gọi hh khí ban đầu là X và hh khí sản phẩm là Y.
\(d_{\dfrac{X}{H_2}}=3,6\rightarrow M_X=3,6.2=7,2\left(\dfrac{g}{mol}\right)\)
Ta có:
\(\dfrac{n_{N_2}}{n_{H_2}}=\dfrac{7,2-2}{28-7,2}=\dfrac{5,2}{20,8}=\dfrac{1}{4}\) ( quy tắc đường chéo )
Gọi x là số mol N2 tham gia phản ứng.
PTHH:
\(N_2+3H_2\xrightarrow[Fe]{t^o}2NH_3\)
Trc p/ư: 1 4
p/ư: x 3x 2x (mol)
sau p/ư: 1-x 4-3x 2x
\(\rightarrow n_Y=1-x+4-3x+2x=5-2x\left(mol\right)\)
\(d_{\dfrac{Y}{H_2}}=4,5\rightarrow M_Y=4,5.2=9\left(\dfrac{g}{mol}\right)\)
BTKL: mX = mY
\(m_Y=1.28+4.2=36\left(g\right)\)
\(\rightarrow\dfrac{36}{9}=5-2x\)
\(\rightarrow x=0,5\)
Giả sử phản ứng xảy ra hoàn toàn:
\(\dfrac{1}{1}< \dfrac{4}{3}\) --> N2 hết, H2 dư.
Trước:
\(\%V_{N_2}=\dfrac{1.22,4}{5.22,4}.100\%=20\%\)
\(\%V_{H_2}=100\%-20\%=80\%\)
Sau:
\(\%V_{NH_3}=\dfrac{1.22,4}{4.22,4}.100\%=25\%\)
\(\%V_{N_2}=\dfrac{\left(1-0,5\right).22,4}{4.22,4}.100\%=12,5\left(\%\right)\)
\(\%V_{H_2}=\dfrac{\left(4-1,5\right).22,4}{4.22,4}.100\%=62,5\%\)

Dựa vào MX, ta có tỉ lệ N2 : H2 = 1 : 4
Phương trình: N2 + 3H2
Ban đầu: x 4x
Phản ứng: 0,2x 0,2. 3x
Sau phản ứng: 0,8x 3,4x
Ta có:
2NH3
0
0,4x
0,4x (Chính là hỗn hợp Y)
2NH3 + 3CuO -> 3Cu + 3H2O + N2
0,4x 0,6x
H2 + CuO -> Cu + H2O
3,4x 3,4x
Theo bài ra ta có 0,6x + 3,4x = 4x = 0,51 mol
=> x = 0,1275
=> V = 0,1275 . 5 . 22,4 = 14,28
=> Đáp án A

Đáp án B
Hỗn hợp ban đầu chứa N 2 : 0 , 2 H 2 : 0 , 8
→ Hiệu suất tính theo N2.
nsau = 3,6/4 = 0,9 → N2 phản ứng = 0,05 → H = 25%

BTKL: mY = mX = 0,4.2 + 0,2.26 = 6 (g)
=> \(n_Y=\dfrac{6}{7,5.2}=0,4\left(mol\right)\)
mH2(pư) = nX - nY = (0,4 + 0,2) - 0,4 = 0,2 (mol)
Gọi số mol Br2 pư là a (mol)
Bảo toàn liên kết: 2.0,2 = 0,2 + a
=> a = 0,2 (mol)
=> mBr2 = 0,2.160 = 32 (g)

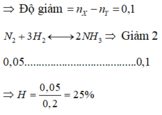


Coi n X = 1(mol)
Gọi n H2 = a(mol) ; n N2 = b(mol)
Ta có :
a + b = 1
2a + 28b = 3,6.2 = 7,2
=> a = 0,8 ; b = 0,2
3H2 + N2 \(\xrightarrow{t^o,xt}\)2 NH3
3a........a..............2a........(mol)
Vì n H2 / 3 > n N2 / 1 nên hiệu suất tinh theo số mol N2
Gọi hiệu suất là a => n N2 pư = a(mol)
m Y = m X = 7,2
=> n Y = 7,2/(4,2826.2) = 0,84(mol)
Sau phản ứng, Y gồm :
H2 : 0,8 - 3a
N2 : 0,2 - a
NH3 : 2a
=> n Y = 0,8 - 3a + 0,2 -a + 2a = 0,84
=> a = 0,08 = 8%