160ml = nhiêu lít
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đây chỉ là một bài toán về kim loại Cu tác dụng với dung dịch có chứa NO3- và H+ đơn giản.
Để giải quyết bài này ta chỉ cần sử dụng đến phương trình ion thu gọn để giải quyết.
Thí nghiệm 1: ta có:
![]()
Xét phản ứng: 3Cu + 2NO3- + 8H+ → 3 C u 2 + +2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,16
Phản ứng: 0,06 0,04 0,16 0,04
Sau phản ứng: 0,06 0,12 0 0,04
Thí nghiệm 2: ta có:
![]()
Xét phản ứng: 3Cu + 2 N O - 3 + 8 H + → 3 C u 2 + + 2NO + 4 H 2 O
Ban đầu: 0,12 (mol) 0,16 0,32
Phản ứng: 0,12 0,08 0,32 0,08
Sau phản ứng: 0 0,08 0 0,08
Ta thấy:
![]()
Đáp án C.



Đáp án A
nOH-- = 0,032 , nH+ = 0,034
H+ dư = 0,034 – 0,032 = 0,002 mol
⇒ [H+] = 0,002 : 0,2 = 0,01⇒ pH = 2.
Đáp án A.

\(m_{H_2O}=160:1=160\left(g\right)\)
\(\Rightarrow C\%_{ddKOH}=\dfrac{14.100\%}{160}=8,75\%\)
\(C\%_{ddOH}=\dfrac{14}{14+1.160}.100\approx8,046\%\)

ta có D=m/V=> m=D.V=1,31.160=209,6g
=> m =209.6g là khối lượng dd H2SO4
=> mH2OS4 =\(\frac{40.209,6}{100}=83,84\)g
=> nH2SO4=0,86 mol

nNaOH = 0,032 (mol) => nOH- = 0,032 (mol)
nAl2(SO4)3 = 0,05 (mol) => nAl3+ = 0,1 (mol)
\(Al^{3+}+3OH^-\left(0,032\right)\rightarrow Al\left(OH\right)_3\downarrow\left(\dfrac{0,032}{3}\right)\)
=> m kết tủa = 0,832 (g)

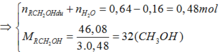
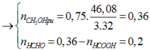
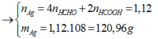
=16 lít
160ml=0,16l