Bài tập 1: Đốt cháy 6,2g P trong bình chứa 6,72 l khí O ( đktc) hãy cho biết sau khi cháy :
a, P hay O chất nào còn thừa và khối lượng là bao nhiêu ?
b, Chất nào được tạo thành và khối lượng là bao nhiêu ?
Bài tập 2: Cho 11,2g Fe tác dụng với 18,2g HCL.Thì sau phản ứng thu được những chất nào. Khối lượng là bao nhiêu gam ?

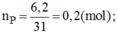
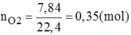
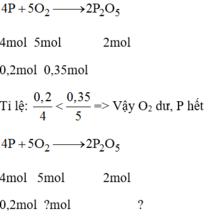
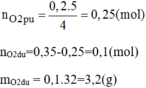
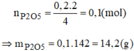
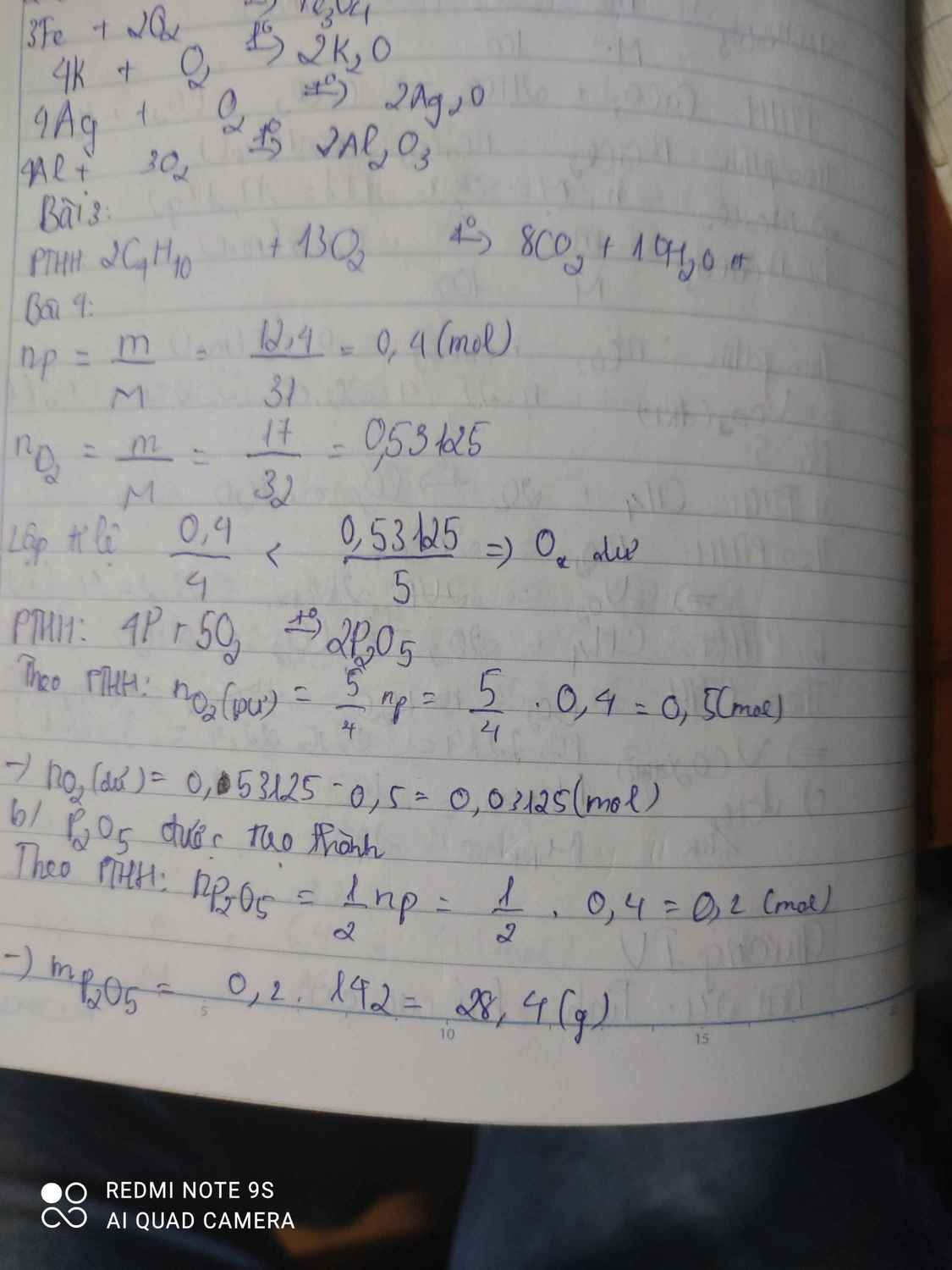

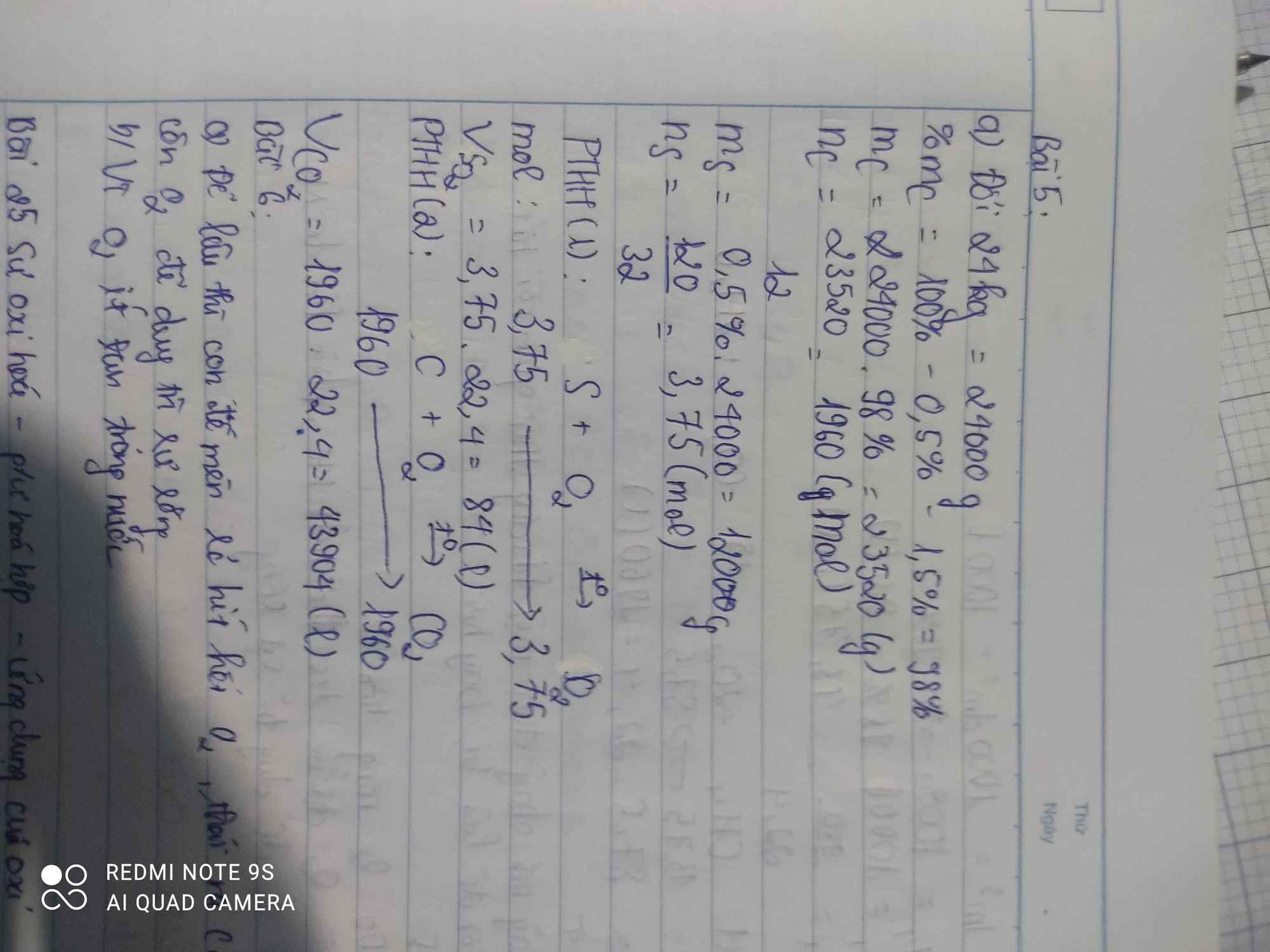
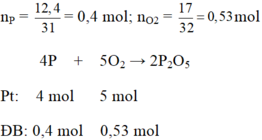

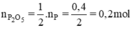
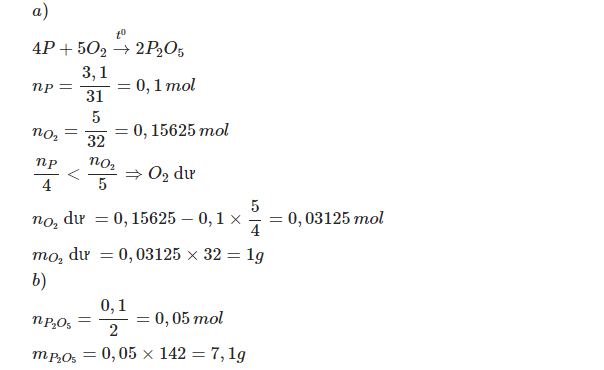
\(a) n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ \dfrac{n_P}{4} = 0,05 < \dfrac{n_{O_2}}{5}=0,06 \to O_2\ dư\\ n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)\\ m_{O_2\ dư} = (0,3 - 0,25).32 = 1,6(gam)\\ b) P_2O_5\ \text{được tạo thành}\\ n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ m_{P_2O_5} = 0,1.142 = 14,2(gam)\)
mơn