Câu 3:
a) Trình bày 5 phương trình phản ứng có thể tạo ra HCl trực tiếp từ Cl2.
b) Bằng các PTPƯ hãy chứng minh axit clohiđric có thể tham gia các phản ứng với vai trò là:
- Chất khử.
-Chất oxi hóa.
-Chất trao đổi (trong phản ứng trao đổi).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

HCl: thể hiện tính oxi hóa với H+; thể hiện tính khử với Cl- và đóng vai trò là môi trường.

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
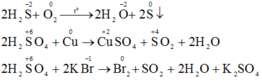

HCl 2 HCl + Fe → FeCl 2 + H 2 4 HCl + MnO 2 → MnCl 2 + Cl 2 + 2 H 2 O

PT:
Fe + S-->FeS (to)
FeS + H2SO4-->H2S + FeSO4
Vai trò:chất oxi hóa

Chọn đáp án B
1. Đúng.
2. Sai.HF là axit rất yếu.Ăn mòn thủy tinh là tính chất riêng có.
3. Sai.Tính khử và tính axit tăng dần
4. Sai điều chế bằng điện phân dung dịch NaCl không có màng ngăn.
5. Sai HClO là axit rất yếu
$a\bigg)$
$Cl_2+H_2O\leftrightharpoons HCl+HClO$
$CH_4+Cl_2\xrightarrow{ánh\, sáng}CH_3Cl+HCl$
$CH_3Cl+Cl_2\xrightarrow{ánh\, sáng}CH_2Cl_2+HCl$
$CH_2Cl_2+Cl_2\xrightarrow{ánh\, sáng}CHCl_3+HCl$
$CHCl_3+Cl_2\xrightarrow{ánh\, sáng}CCl_4+HCl$
$b\bigg)$
- Chất khử:
$2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2+8H_2O$
- Chất oxi hóa:
$Fe+2HCl\to FeCl_2+H_2$
- Chất trao đổi:
$AgNO_3+HCl\to AgCl\downarrow+NaNO_3$
bạn ơi cho mình hỏi bn đc ko