Các muối tạo thành trong dung dịch sau khi sục 22,4 lit khí Hidro sunfua (đktc) vào 280 gam dung dịch KOH 40% là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn B
nH2SO4 = 0,49 mol > nH2 = 0,25 mol => axit dư
=> Fe ; Al hết. Chất rắn là Cu
=> mFe + mAl = 56nFe + 27nAl = 17,9 – 9,6 = 8,3g
nH2 = nFe + 1,5nAl = 0,25 mol
=> nFe = nAl = 0,1 mol.
nH2SO4 dư = 0,49 – 0,25 = 0,24 mol => nH+ = 0,48 mol
Khi thêm 0,12 mol NaNO3 vào thì Cu( 0,15 mol) và Fe2+ phản ứng
3Cu + 8H+ + 2NO3- -> 3Cu2+ + 2NO + 4H2O
0,15->0,4 -> 0,1 mol
3Fe2+ + 4H+ + NO3- -> 3Fe3+ + NO + 2H2O
0,06<- 0,08 -> 0,02
=> VNO = 0,12.22,4 = 2,688 lit
Vậy trong dung dịch sau có : 0,06 mol Fe3+ ; 0,04 mol Fe2+ ; 0,15 mol Cu2+ ; 0,1 mol Al3+ ; 0,49 mol SO42-; 0,12 mol Na+
=> m = 67,7g

Chị nghĩ đề là 2,24 sẽ hợp lý hơn nhé! Còn nếu em vẫn để số liệu là 2,688 thì hướng làm vẫn như vậy chỉ là số liệu khác nhưng mà chị tính hiện tại theo số liệu của em thì không ra.
Bài làm
\(\begin{array}{l}
{n_{C{O_2}}} = \dfrac{{2,24}}{{22,4}} = 0,1mol\\
C{O_2} + KOH \to KHC{O_3}\\
C{O_2} + 2KOH \to {K_2}C{O_3}\\
hh:KHC{O_3}(a\,mol),{K_2}C{O_3}(b\,mol)\\
\left\{ \begin{array}{l}
a + b = 0,1mol\\
100a + 138b = 11,4
\end{array} \right.\\
\Rightarrow a = 0,06;b = 0,04\\
{n_{KOH}} = {n_{KHC{O_3}}} + 2{n_{{K_2}C{O_3}}} = 0,14mol\\
{m_{KOH}} = 0,14 \times 56 = 7,84g\\
C{\% _{KOH}} = \dfrac{{7,84}}{{150}} \times 100\% = 5,227\% \\
C{\% _{KHC{O_3}}} = \dfrac{{0,06 \times 100}}{{0,1 \times 44 + 150}} \times 100\% = 3,88\% \\
C{\% _{{K_2}C{O_3}}} = \dfrac{{0,04 \times 138}}{{0,1 \times 44 + 150}} \times 100\% = 3,575\%
\end{array}\)

Chọn B
n C O 2 = 0,075 mol
Vì KOH dư nên phản ứng tạo ra muối trung hòa
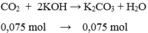
Vì thể tích dung dịch trước và sau không thay đổi


\(a)\\ Fe + 2HCl \to FeCl_2 + H_2\)
b)
\(n_{Fe} = \dfrac{22,4}{56}= 0,4(mol)\\ n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\)
Ta thấy : \(n_{Fe} > n_{H_2}\) nên Fe dư.
Theo PTHH :
\(n_{Fe\ pư} = n_{H_2} = 0,3(mol)\\ \Rightarrow m_{Fe\ pư} = 0,3.56 = 16,8(gam)\)
c)
Ta có :
\(n_{FeCl_2} = n_{H_2} = 0,3(mol)\\ \Rightarrow m_{FeCl_2} = 0,3.127 = 38,1(gam)\)

Chọn D.
Tiến hành các thí nghiệm, phương trình hóa học tương ứng xảy ra là:
Kết thúc, có tất cả 4 thí nghiệm thu được muối trung hòa.

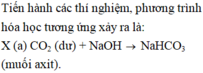
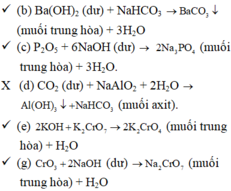

\(n_{H_2S} = \dfrac{22,4}{22,4} = 1(mol)\\ n_{KOH} = \dfrac{280.40\%}{56} = 2(mol) = 2n_{H_2S}\)
Suy ra : muối tạo thành chỉ có K2S
\(2KOH + H_2S \to K_2S + 2H_2O\)