Cho a gam Ba vào 200 ml dung dịch X gồm Ba(OH), 0,1M và KOH 0,3M. Sau phản ứng thu được dung dịch Y và V lít khí (dktc). Cho từ từ dung dịch Y vào 100 ml dung dịch A*l_{2} * (S*O_{4}) 0,25M thu được kết tủa Z. Lọc tách kết tủa Z nung đến khối lượng không đổi thu được 9,03 gam chất rắn. 1. Viết các phương trình phản ứng xảy ra? 2. Tính a, V?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


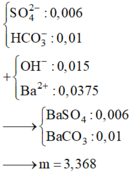
Dung Dịch X có 0,012 mol CO32- ; 0,006 mol HCO3-
Dung dịch Y có 0,012 mol
H+ pt H+ + CO3 → HCO3
0,02 0,012 0,012 (mol)
H+ + HCO3 → CO2
0,08 0,08 0,08 (mol)
V= 0,08.22,4 = 0,1792 l = 179,2 ml
dung dịch Z còn 0,01mol HCO3 ; 0,006 mol SO4 Ba2+ và OH- dư
m kết tủa = 0,006.(137+96)+ (0,01.137+60)= 3,368g =>B

Chọn đáp án D
nH2SO4 = 0,156x0,5 = 0,078 Þ nH+ = 0,078x2 = 0,156
Cho từ từ 0,156 H+ vào

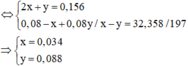
Vậy V = (0,034 + 0,088)x22,4=2,7328

Đáp án A
![]()
Cho từ từ đến X vào 0,02 ml HCl thu được 0,015 mol khí CO2
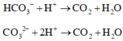
Giải được số mol HCO3- và CO32- phản ứng là 0,1 và 0,05 mol.
Do vậy trong X HCO3- và CO32- có tỉ lệ số mol là 2:1.
Vì còn CO32- nên kết tủa thu được là BaCO3 0,02 mol.
X chứa NaHCO3 và Na2CO3 với số mol lần lượt là 0,02 và 0,01 mol.
![]()

Đáp án D
+ Ba ( OH ) 2 ⏟ 0 , 02 mol + NaHCO 3 ⏟ 0 , 03 mol → BaCO 3 ↓ ⏟ 0 , 02 mol + OH - : 0 , 01 mol CO 3 2 - : 0 , 01 mol Na + : 0 , 03 mol ⏟ dd X + Cho từ từ HCl vào X đến khi bắt đầu thoát khí ra 2 phản ứng : H + + OH - → H 2 O H + + CO 3 2 - → HCO 3 - ⇒ n H + = 0 , 02 ⇒ V HCl = 0 , 02 . 1000 0 , 25 = 80 ml