Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
hhM gồm CnH2n - 2 và H2 có dM/CH4 = 0,6.
Nung M với Ni → hhN có N/CH4 = 1.
• Ta có hhN có M = 16 → H2 dư.
Đặt nCnH2n - 2 x mol và H2 y mol.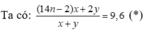
Vì phản ứng xảy ra hoàn toàn → hhN gồm CnH2n + 2 x mol và H2 dư (y - 2x) mol.![]()
Từ (*), (**) → y = 4x → n = 3 → CH≡C-CH3 → metylaxetilen

PTHH: \(2Al+3S\underrightarrow{^{t^o}}Al_2S_3\)
Gọi số mol Al là x; S là y.
Ta có phương trình : \(27x+32y=10,2\left(g\right)\)
Vì cho Y tác dụng với HCl thu được hỗn hợp khí nên Al dư
\(\Rightarrow n_{Al_2S_3}=\dfrac{1}{3}n_S=\dfrac{y}{3}\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=x-\dfrac{2y}{3}\left(mol\right)\)
PTHH:
\(Al_2S_3+6HCl\rightarrow2AlCl_3+3H_2S\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow n_{H2S}=3n_{Al2S3}=y\left(mol\right);n_{H2}=\dfrac{3}{2}n_{Al}=1,5x-y\left(mol\right)\)
\(M_Z=18\)
Áp dụng quy tắc đường chéo :
\(\Rightarrow\dfrac{n_{H2S}}{n_{H2}}=\dfrac{16}{16}\Rightarrow1,5x-y=y\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{5,4}{10,2}=52,94\%\\\%m_S=100\%-52,94\%=47,06\%\end{matrix}\right.\)

5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)

\(H_2+Cl_2\rightarrow2HCl\)
Vì phản ứng hoàn nên nên một trong 2 chất là H2 hoặc Cl2 phải hết.
Ta có: \(M_X=15M_{H2}=30< M_{HCl}=36,5\rightarrow X\text{ chứa }H2\rightarrow H2\text{dư}\)
Vậy X gồm H2 và HCl

Xét `a<b->H` tính theo `Fe.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5a->0,5a->0,5a(mol)`
Có `n_{Fe\ pu}=0,5a(mol)`
`Y` gồm `Fe:0,5a(mol);S:b-0,5a(mol);FeS:0,5a(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5a(mol);n_{H_2}=n_{Fe}=0,5a(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5a}/{0,5a}=1/3` vô lí.
Xét `a>b->H` tính theo `S.`
`Fe+S` $\xrightarrow{t^o}$ `FeS`
`0,5b←0,5b->0,5b(mol)`
Có `n_{S\ pu}=0,5b(mol)`
`Y` gồm `Fe:a-0,5b(mol);S:0,5b(mol);FeS:0,5b(mol)`
`FeS+2HCl->FeCl_2+H_2S`
`Fe+2HCl->FeCl_2+H_2`
Theo PT: `n_{H_2S}=n_{FeS}=0,5b(mol);n_{H_2}=n_{Fe}=a-0,5b(mol)`
`->{n_{H_2S}}/{n_{H_2}}={5.2-2}/{34-5.2}=1/3`
``->{0,5b}/{a-0,5b}=1/3`
`->1,5b=a-0,5b`
`->a=2b`
`->a:b=2:1`

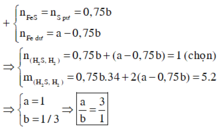
\(H_2+Cl_2\rightarrow2HCl\)
X chắc chắn có : HCl
\(\overline{M}=9.625\cdot2=19.25\left(\dfrac{g}{mol}\right)\)
=> X chứa : H2 dư
\(Giảsử:n_A=1\left(mol\right)\)
\(n_{Cl_2}=a\left(mol\right)\Rightarrow n_{H_2}=1-a\left(mol\right)\)
\(\overline{M}=\dfrac{36.5\cdot2a+\left(1-2a\right)\cdot2}{1-2a+2a}=19.25\)
\(\Rightarrow a=0.25\)
\(\%H_2=\dfrac{1-0.25}{1}\cdot100\%=75\%\)
Chúc học tốt <3
Ôi cảm ơn b nhiều lắm, b có thể giúp mình thêm 1 câu nữa đc k?