Phương pháp điều chế khí clo trong công nghiệp là
A. điện phân dung dịch NaCl có màng ngăn xốp
B. điện phân dung dịch NaCl
C. điện phân dung dịch KCl có màng ngăn
D. cho HCl tác dụng với chất oxi hóa mạnh
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Trong công nghiệp, để điều chế các kim loại kiềm người ta tiến hành điện phân nóng chảy muối clorua của chúng.
KCl → t 0 K + ½ Cl2

TK
a) Phương trình hóa học: Na2CO3 + Ca(OH)2 → CaCO3 + 2NaOH
b) Số mol NaOH điều chế được: nNaOH = 2nNa2CO3 =0,25. 2 = 0,5 mol

Đáp án A.
Tại catot: Cu2+: a mol; Na+: b mol;
Cu2+ + 2e → Cu
a ⟶ 2a
Hết Cu2+: 2H2O+2e→2OH−+H2
Tại anot: Cl−: b mol; SO2−4: a mol; H2O
2Cl−→Cl2+2e
b ⟶ b
Hết Cl−: 2H2O − 4e→4H++O2
Vì dung dịch sau điện phân làm phenolphtalein chuyển sang màu hồng chứng tỏ ở catot Cu2+ hết trước Cl− ở anot, còn ở anot Cl− vẫn điện phân ⟹ 2a < b

Chọn đáp án B
Ta có:
![]()
![]()
BTNT.Clo → Khí thoát ra ở cực dương phải là Cl2 và O2 .
Ta có
![]()
![]()
Và
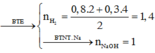
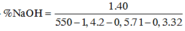
=7,96%

Đáp án A
Điện phân dung dịch NaCl và HCl (điện cực trơ, màng ngăn xốp). Trong quá trình điện phân, so với dung dịch ban đầu thì giá trị pH của dung dịch thu được tăng lên. Lúc đầu dung dịch có pH nhỏ hơn 7, trong quá trình điện phân, HCl bị điện phân trước làm nồng độ H+ giảm nên pH bắt đầu tăng, khi H+ bị điện phân hết thì dung dịch có pH = 7. Tiếp đó NaCl bị điện phân làm cho nồng độ O H - tăng lên và pH tiếp tục tăng lên lớn hơn 7.
2 H C l → đ i ệ n p h â n d u n g d ị c h H 2 + C l 2 2 N a C l + H 2 O → c ó m à n g n g ă n x ố p đ i ệ n p h â n d u n g d ị c h 2 N a O H + H 2 ↑ + C l 2 ↑

2NaCl + 2H2O đpdd→ 2NaOH + H2 + Cl2
Do không có màng ngăn Cl2 sinh ra tác dụng với NaOH
Cl2 + 2NaOH → NaCl + NaClO + H2O ( nước giaven)
=> Chọn D

Đáp án A
mdung dịch = 200.1,1 = 220 (g); nNaOH = nNaCl = 0,2.2 = 0,4 (mol)
dễ thấy khí thoát ra ở catot là H2 với = 1 (mol)

Đáp án : A