Dung dịch E chứa các ion: Ca2+, Na+, HCO3-, Cl- trong đó số mol của Cl- gấp đôi số mol của ion Na+. Cho một nửa dung dịch E phản ứng với dd NaOH dư thu được 4g kết tủa. Cho một nửa dd E còn lại phản ứng với dd Ca(OH)2 dư thu được 5g kết tủa. Mặt khác, nếu đun sôi đến cạn dung dịch E thu được m gam chất rắn khan. Giá trị của m là:
A. 11,84
B. 8,79
C. 7,52
D. 7,09


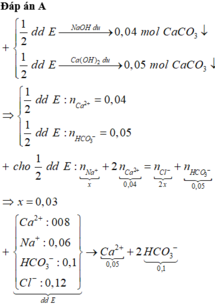


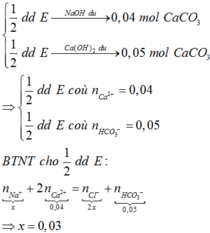
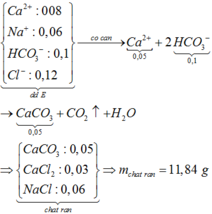


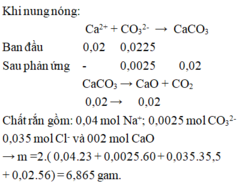


Đáp án A
Đặt Ca2+: a mol có trong 1/2dung dịch
Na+: b mol
HCO3-: c mol
Cl-: 2b mol
1/2 dung dịch X tác dụng NaOH dư
HCO3- + OH- → CO32- + H2O
c c
CO32- + Ca2+ → CaCO3
c a 0,04
1/2 dung dịch X tác dụng Ca(OH)2 dư
HCO3- + OH- → CO32- + H2O
c c
CO32- + Ca2+ → CaCO3
c c = 0,05
Ta có: nCaCO3↓ lần đầu = 0,04 mol và sau = 0,05
=> c = 0,05 mol và a = 0,04
Bão toàn mol điện tích ta có: 2a + b = c + 2b => b = 0,03
Đun sôi dung dịch đến cạn
2HCO3− → H2O + CO2 + CO32−
0,05 → 0,025
m chất rắn =(40a + 23b + 60c/2 + 35,5 . 2 . 0,03) . 2 = 11,84g