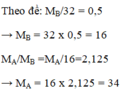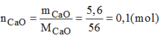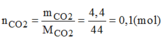Câu 4: (2đ)
a , Tìm khối lượng mol khí A, biết khí A có tỉ khối với khí hidro là 16. Cho biết B là khí nào sau đây: N2, CO2, SO2, O2 .
b, Phân hủy 50 g Canxi cacbonat (CaCO3) ở nhiệt độ cao thu được 28 g CaO và khí CO2.Hãy tính thể tích (ở đktc) của khí CO2 thu được?
giúp mik vs ! cần gấp lắm ạ