Thổi 1 luồng khí CO dư qua ống sứ đựng m gam hỗn hợp gồm: CuO, Fe2O3, FeO, Al2O3 nung nóng thu được 2,5g chất rắn. Toàn bộ khí sinh ra sục vào nước vôi trong dư thấy có 15g kết tủa trắng. Khối lượng các oxit kim loại ban đầu là: (biết các phản ứng xảy ra hoàn toàn)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2\\ CuO + CO \xrightarrow{t^o} Cu + CO_2\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO} = n_{CO_2} = n_{CaCO_3} = \dfrac{15}{100} = 0,15(mol)\\ \Rightarrow m = m_Y + m_{CO_2} - m_{CO} = 200 + 0,15.44 - 0,15.28 = 202,4(gam)\)

A
Ta có nO = nCaCO3 = 1,5.10-3.
Vậy m = 2,15 + 16. 1,5.10-3 = 2,174 gam

Các phương trình hóa học:
MxOy + yCO → xM + yCO2
Ca(OH)2 + CO2 → CaCO3 + H2O
Ta có: moxit = mkim loại + moxi
Trong đó:
→moxit = 2,5 + 0,15.16 = 4,9 gam
Các phương trình hóa học:
MxOy + yCO → xM + yCO2
Ca(OH)2 + CO2 → CaCO3 + H2O
Ta có: moxit = mkim loại + moxi
Trong đó:
→moxit = 2,5 + 0,15.16 = 4,9 gam

nCaCO3 = \(\dfrac{15}{100}=0,15\left(mol\right)\)
Pt: CuO + CO --to--> Cu + CO2 (1)
......Fe2O3 + 3CO --to--> 2Fe + 3CO2 (2)
......FeO + CO --to--> Fe + CO2 (3)
......CO2 + Ca(OH)2 --> CaCO3 + H2O
...0,15 mol<--------------0,15 mol
Theo pt (1),(2) và (3): nCO pứ = nCO2 = 0,15 mol
=> nO oxit = nO (CO pứ) = 0,15 mol
m = 0,15 . 16 + 2,5 = 4,9 (g)

Đối với bài này áp dụng định luật BTKL để giải.
Oxit + CO \(\rightarrow\) Kim loại + CO2
...........0,15.......................0,15
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3
0,15............................0,15
Áp dụng BTKL ta có
m + mCO = mCO2 + 215
=> m + 0,15*28 = 0,15*44 +215
=> m =217,4 gam
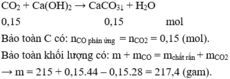
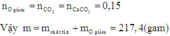
\(CO+hh_{oxit}\rightarrow hh_{ran}+CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Ta có kết tủa trắng là CaCO3 0,15 mol \(\rightarrow\) nCO2=0,15 mol
Từ CO \(\rightarrow\) CO2 do đó CO đã lấy 1 O của hỗn hợp oxit
\(\Rightarrow n_{O_{bi.khu}}=n_{CO2}=0,15\left(mol\right)\)
\(\Rightarrow m=16+0,15.16=18,4\left(g\right)\)