Câu 1: Dẫn 0,1 mol khí axetilen qua dung dịch nước brom dư. Khối lượng brom tham gia phản ứng là
A. 16,0 gam. B. 20,0 gam.
C. 26,0 gam. D. 32,0 gam.
Câu 2: Đốt cháy hoàn toàn 5,6 lít khí C2H2 trong bình chứa khí oxi dư. Thể tích khí CO2 thu được (trong cùng điều kiện nhiệt độ và áp suất) là
A. 11,2 lít. B. 16,8 lít.
C. 22,4 lít. D. 33,6 lít.
Câu 3: Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu lần lượt là
A. 20%; 80%. B. 30%; 70%.
C .40% ; 60%. D. 60%; 40%.


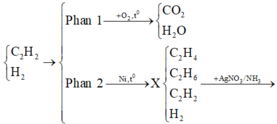
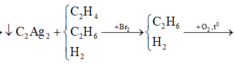
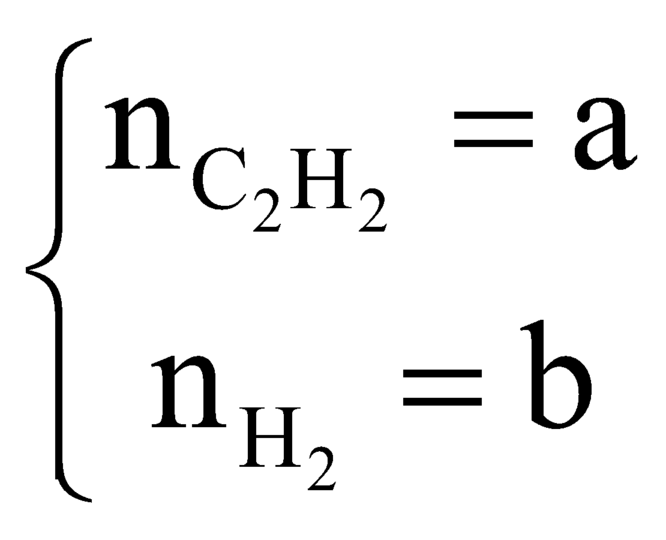
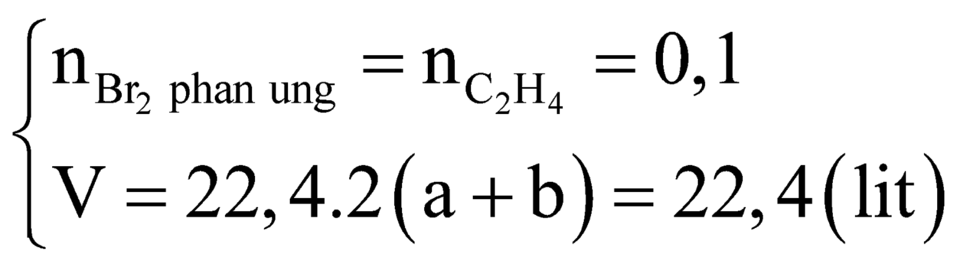
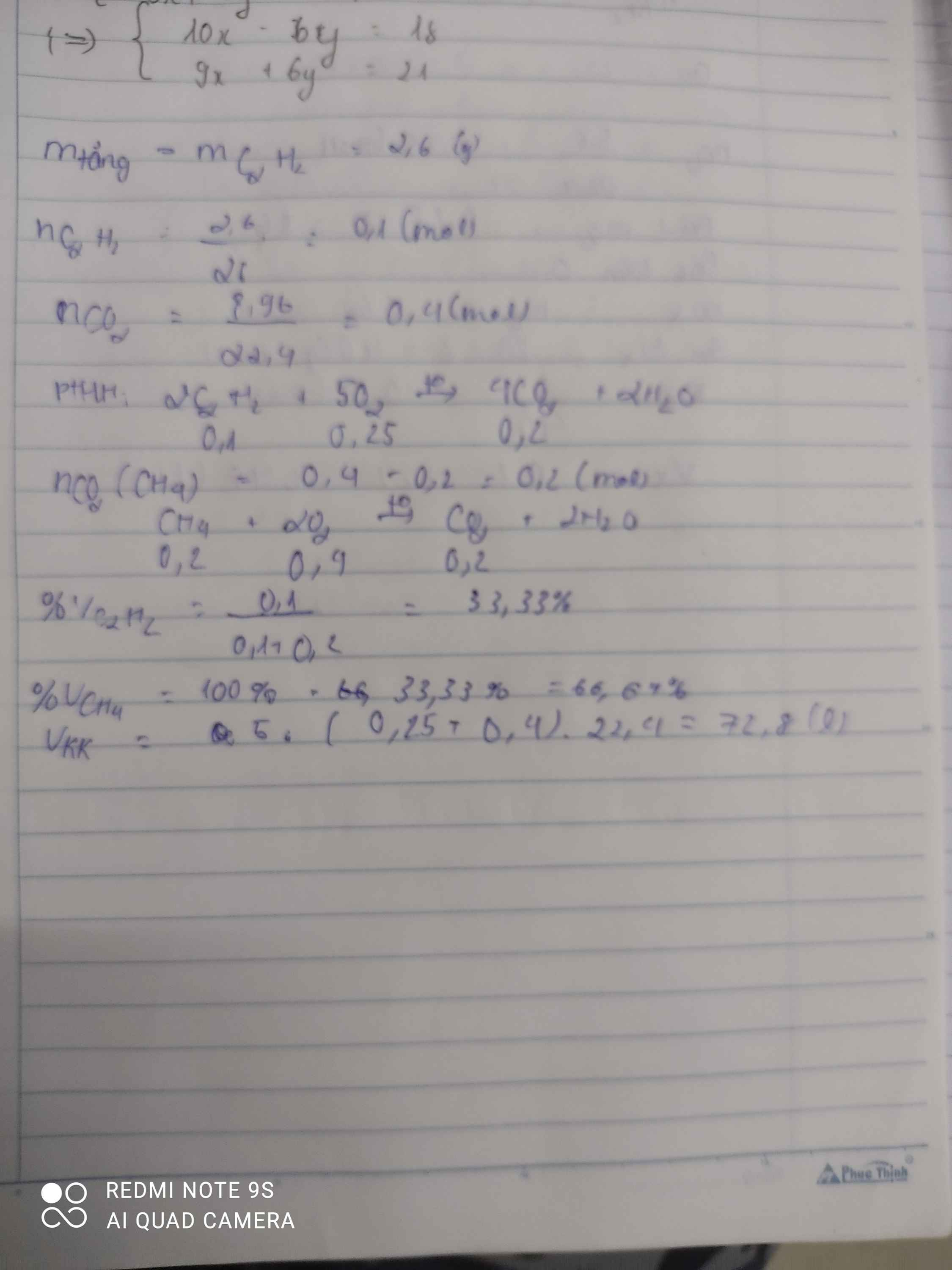

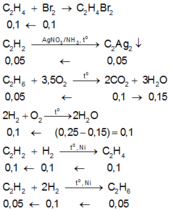
Câu 1: A
Câu 2: A
Câu 3: B
Câu 1: Dẫn 0,1 mol khí axetilen qua dung dịch nước brom dư. Khối lượng brom tham gia phản ứng là
A. 16,0 gam. B. 20,0 gam.
C. 26,0 gam. D. 32,0 gam.
Câu 2: Đốt cháy hoàn toàn 5,6 lít khí C2H2 trong bình chứa khí oxi dư. Thể tích khí CO2 thu được (trong cùng điều kiện nhiệt độ và áp suất) là
A. 11,2 lít. B. 16,8 lít.
C. 22,4 lít. D. 33,6 lít.
Câu 3: Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu lần lượt là
A. 20%; 80%. B. 30%; 70%.
C .40% ; 60%. D. 60%; 40%.