Câu 1: viết các phương trình phản ứng xảy ra cho các sơ đồ saua,HCl→Cl2→FeCl3→NaCl→HCl→CuCl2→AgClb,KMnO4→Cl2→HCl→FeCl3→AgCl→Cl2→Br2→I2→ZnI2→Zn(OH)2c,MnO2→Cl2→KClO3→KCl→HCl→Cl2→Clorua vôiCâu 2: Nhận biết các dạng dung dịch mất nhãn sau bằng phương pháp hóa học :NaCl,NaBr,NaI,HCl,H2SO4,NaOH.Câu 3: Cho 31,6 g KMnO4 tác dụng với dung dịch HCl dư sẽ thu được bao nhiêu lít Cl2(ở đktc) nếu H của phản ứng là 75 %Câu 4: Cho 8,3 gam hỗn hợp...
Đọc tiếp
Câu 1: viết các phương trình phản ứng xảy ra cho các sơ đồ sau
a,HCl→Cl2→FeCl3→NaCl→HCl→CuCl2→AgCl
b,KMnO4→Cl2→HCl→FeCl3→AgCl→Cl2→Br2→I2→ZnI2→Zn(OH)2
c,MnO2→Cl2→KClO3→KCl→HCl→Cl2→Clorua vôi
Câu 2: Nhận biết các dạng dung dịch mất nhãn sau bằng phương pháp hóa học :NaCl,NaBr,NaI,HCl,H2SO4,NaOH.
Câu 3: Cho 31,6 g KMnO4 tác dụng với dung dịch HCl dư sẽ thu được bao nhiêu lít Cl2(ở đktc) nếu H của phản ứng là 75 %
Câu 4: Cho 8,3 gam hỗn hợp Al,Fe,Mg tác dụng hết với dung dịch HCl vừa đủ .Sau phản ứng khối lượng dung dịch HCl tăng thêm 7,8 gam . Tính khối lượng muối thu được.
Câu 5: Hỗn hợp khí X gồm o6zon và oxi có tỉ khối đối với hidro bằng 17,2. Tính phần trăm theo thể tích mỗi khí trong hỗn hợp X.
Câu 6:Cho 9 gam hỗn hợp gồm Al và Cu tác dụng với lượng dư dung dịch HCl nồng độ 20% . Sau phản ứng thu được 1,344 lít khí (ở đktc).
a, Tính % về khối lượng các kim loại trong hỗn hợp ban đầu
b,Tính khối lượng dung dịch HCl đã dùng . Biết rằng lượng dung dịch HCl đã dùng được lấy dư 10% so với lượng cần thiết cho phản ứng.




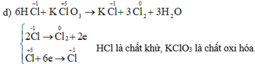
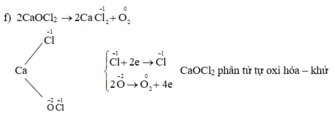

 3)
3)

a) HCl(đ) + MnO2 -t0-> Cl2 + MnCl2 + H2O
b) CuO + 2HCl - > CuCl2 + H2O
c) 2HCl + Na2Co3 -> CO2 + 2NaCl + H2O
d) HCl + AgNO3 - > AgCl + HNO3
e) 2KCl + 2H2O \(\xrightarrow[cmn]{đpdd}\) 2KOH + Cl2 + H2
f) Cl2 + H2O - > HCl + HClO
Cl2 + NaOH - > NaCl + NaClo
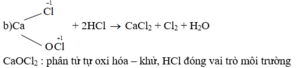
g Cl2 + Ca(OH)2 -t0->CaoCl2 + H2O
h) 2CaOCl2+ H2O + CO2 - > CaCO3 + CaCl2 +2HClO
NaClo + CO2 + H2O - > NaHCO3 + HClO